题目内容
对于反应2SO2(g)+O2(g)?2SO3(g)△H<0,下列判断正确的是( )
| A、2体积SO2和足量O2反应,必定生成2体积SO3 |
| B、其他条件不变,增大压强,平衡必定向右移动 |
| C、平衡时,SO2消耗速率必定等于O2的生成速率 |
| D、平衡时,SO2浓度必定等于O2浓度的两倍 |
考点:化学平衡的影响因素,化学平衡状态的判断
专题:化学平衡专题
分析:A、可逆反应的反应物不能完全转化;
B、加压平衡向气体体积减小的方向移动;
C、反应速率之比等于化学计量数之比;
D、平衡状态时各物质浓度比的大小决定于开始加入物质的多少.
B、加压平衡向气体体积减小的方向移动;
C、反应速率之比等于化学计量数之比;
D、平衡状态时各物质浓度比的大小决定于开始加入物质的多少.
解答:
解:A、2体积SO2和足量O2反应,必定生成小于2体积的SO3,故A错误;
B、加压平衡向气体体积减小的正方向移动,故B正确;
C、平衡时,SO2消耗速率与O2的生成速率之比为2:1,故C错误;
D、平衡状态时各物质浓度比的大小决定于开始加入物质的多少,故D错误;
故选B.
B、加压平衡向气体体积减小的正方向移动,故B正确;
C、平衡时,SO2消耗速率与O2的生成速率之比为2:1,故C错误;
D、平衡状态时各物质浓度比的大小决定于开始加入物质的多少,故D错误;
故选B.
点评:本题考查了可逆反应不能完全转化以及反应速率、平衡状态等等,注重了基础知识的考查,注意对基础知识的理解掌握,本题难度不大.

练习册系列答案
相关题目
下列实验方法或数据合理的是( )
| A、用10mL量筒量取7.50mL稀盐酸 |
| B、用25mL碱式滴定管准确量取22.00mL的KMnO4溶液 |
| C、用广泛pH试纸测出某盐酸溶液的pH为3.2 |
| D、用托盘天平准确称取9.8gNaCl 固体 |
下列叙述或表示正确的是( )
| A、0.1 mol?L-1的醋酸的pH=a,0.01 mol?L-1的醋酸的pH=b,则a+1=b |
| B、用200 mL 4 mol?L-1的NaOH溶液将0.6 mol CO2完全吸收,反应的离子方程式为:3CO2+4OHˉ=CO32ˉ+2HCO3ˉ+H2O |
| C、难溶电解质AB2的饱和溶液中,c(A2+)=xmol?L-1,c(B-)=y mol?L-1,则Ksp值为4xy2 |
| D、常温下0.1 mol?L-1的醋酸溶液与等浓度等体积NaOH溶液反应后的溶液中:c(CH3COOH)+c(CH3COOˉ)=0.1 mol?L-1 |
下列过程最终无沉淀产生的是( )
| A、过量氨气通入Al2(SO4)3溶液 |
| B、过量CO2通入CaCl2溶液 |
| C、少量SO2通入BaCl2溶液后再通入过量Cl2 |
| D、过量CO2通入Na2SiO3溶液 |
下列物质中,属于电解质的是( )
| A、CO2 |
| B、盐酸 |
| C、BaSO4 |
| D、C2H5OH |
下列叙述中,正确的是 ( )
| A、太阳能、核能和天然气都属于新型能源 |
| B、哥本哈根气候大会讨论的减排目标主要是控制二氧化硫排放 |
| C、84消毒液具有强氧化性,可杀死流感病毒 |
| D、比黄金还贵的18O2和普通的16O2是两种不同的核素 |
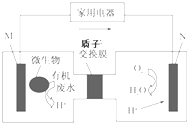 有媒体报道一种新型污水处理装置问世,该装置可利用一种微生物将有机废水的化学能直接转化为电能,该装置的构造如图所示.下列说法中正确的是( )
有媒体报道一种新型污水处理装置问世,该装置可利用一种微生物将有机废水的化学能直接转化为电能,该装置的构造如图所示.下列说法中正确的是( )| A、装置外电路中箭头的方向代表电流的方向 |
| B、该装置为原电池装置,其中N为负极 |
| C、若有机废水中含有葡萄糖,则M电极发生的电极反应式为C6H12O6+6H2O-24e-═6CO2+24H+ |
| D、该处理工艺会导致有机废水酸性增强,仍旧不能直接排放 |
下列关于中和热的说法中正确的是( )
| A、10L 0.05mol?L-1Ba(OH)2溶液与20L0.05mol?L-1HNO3反应时的反应热是中和热 |
| B、1molHCl气体通入1L 0.01mol?L-1NaOH溶液中反应时的反应热是中和热 |
| C、1molHClO与2molNaOH溶液反应时的反应热也可能是中和热 |
| D、只要强酸与强碱在衡溶液中反应生成1mol水时的反应热就是中和热 |