题目内容
10.某温度下,反应SO2(g)+$\frac{1}{2}$(g)?SO3(g)的平衡常数K1=20,在同一温度下,反应2SO3(g)?2SO2(g)+O2(g)的平衡常数K2的值为( )| A. | 400 | B. | 500 | C. | 4×10-4 | D. | 2.5×10-3 |
分析 K与化学计量数为指数关系,互为可逆反应的K为倒数关系,以此来解答.
解答 解:由SO2(g)+$\frac{1}{2}$(g)?SO3(g)的平衡常数K1=20,
可知2SO2(g)+(g)?SO3(g)的平衡常数K=(K1)2=202=400,
则2SO3(g)?2SO2(g)+O2(g)的平衡常数K2=$\frac{1}{K}$=$\frac{1}{400}$=2.5×10-3,
故选D.
点评 本题考查化学平衡的计算,为高频考点,把握化学计量数与K的关系、可逆反应中K的关系为解答的关键,侧重分析与计算能力的考查,注意已知反应与目标反应的关系,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.下列指定反应的离子方程式正确的是( )
| A. | NaHCO3的水解:HCO3-+H2O?CO32-+H3O+ | |
| B. | 用石墨作电解电解氯化镁溶液:2Cl-+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2OH-+H2↑+Cl2↑ | |
| C. | Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-?2Fe2++I2+3H2O | |
| D. | 向Ba(OH)2溶液中加入过量的NH4HSO4溶液:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
17.几种短周期元素的原子半径及主要化合价见表:下列叙述正确的是( )
| 元素符号 | K | L | M | Q | R | T | N |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.152 |
| 主要化合价 | +1 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
| A. | K、L、M三种元素的单质的还原性逐渐增强 | |
| B. | 在RCl2分子中,各原子最外层均满足8电子的稳定结构 | |
| C. | Q元素的最高价氧化物为电解质,其水溶液能够导电 | |
| D. | K在T单质中燃烧所得的化合物中有共价键 |
5.下列说法正确的是( )
| A. | 某盐溶液与NaOH溶液共热,产生使湿润红色石蕊试纸变蓝气体,说明原溶液中存在NH4+ | |
| B. | 某溶液中加入硝酸银溶液时,产生白色沉淀,说明原溶液中含有Cl- | |
| C. | 用铂丝蘸取某溶液在酒精灯上灼烧时,火焰呈黄色,说明原溶液中一定含有NaCl | |
| D. | 某溶液中加入BaCl2溶液生成白色沉淀,说明原溶液中有SO42- |
2.下列说法不正确的是( )
| A. | H2O、H2S、H2Te分子间作用力依次增大 | |
| B. | 金刚石是碳原子间以共价键相结合的原子晶体,加热熔化时需破坏共价键 | |
| C. | 氢氧化钙和氯化铵固体加热制氨气过程中,均有离子键和共价键的断裂和生成 | |
| D. | SiO2和CO2中每个原子的最外层都具有8电子稳定结构 |
19.白磷分子如图所示:则31g白磷中存在的共价键数目为( )

| A. | 4NA | B. | NA | C. | 1.5NA | D. | 0.25NA |
20.对羟基扁桃酸是合成农药、香料等的重要中间体,它可由苯酚和乙醛酸在一定条件下反应制得.
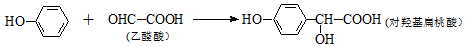
下列有关说法不正确的是( )
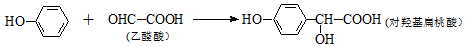
下列有关说法不正确的是( )
| A. | 上述反应的原子利用率可达100% | |
| B. | 上述反应类型为取代反应 | |
| C. | 对羟基扁桃酸可发生加成反应、取代反应和缩聚反应 | |
| D. | 1 mol对羟基扁桃酸与足量NaOH溶液反应,最多可消耗3 mol NaOH |