题目内容
16.已知①氢硫酸是二元弱酸,②CuSO4+H2S═CuS↓+H2SO4.在氢硫酸溶液中,通入或加入少量的下列物质:①O2;②Cl2;③SO2;④CuSO4.能使溶液中的c(H+)增大的是( )| A. | ①② | B. | ②④ | C. | ②③④ | D. | ① |
分析 H2S具有还原性,能被强氧化剂氧化,H2S属于酸,其水溶液呈酸性,能和硫酸铜反应生成难溶于稀硫酸的CuS,据此分析解答.
解答 解:H2S具有还原性,能被强氧化剂氧化,
①2H2S+O2=S↓+2H2O,该反应由酸性变为中性,所以c(H+)减小,故错误;
②H2S+4Cl2+4H2O=H2SO4+8HCl,氢硫酸属于弱酸、硫酸和HCl属于强酸,所以溶液酸性最强,则溶液中c(H+)增大,故正确;
③2H2S+SO2=3S↓+2H2O,溶液由酸性变为中性,则溶液中c(H+)减小,故错误;
④H2S+CuSO4=CuS↓+H2SO4,氢硫酸是弱酸、硫酸是强酸,则溶液酸性最强,溶液c(H+)增大,故正确;
故选B.
点评 本题考查了氢硫酸的性质,根据物质之间的反应分析解答,会正确书写方程式,注意④是中学阶段学习的唯一由弱酸制取强酸的反应,为易错点.

练习册系列答案
相关题目
1.C、H、O三种元素组成的T、X在一定条件下可以发生如下转化: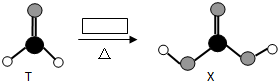
X不稳定,易分解.为使转化能够成功进行,方框内可能加入的试剂是( )

X不稳定,易分解.为使转化能够成功进行,方框内可能加入的试剂是( )
| A. | O2 | B. | NaOH溶液 | C. | 稀硫酸 | D. | Na2SO3溶液 |
5.如图下列表述不正确的是( )
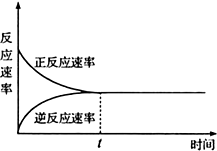

| A. | t时刻表示在给定条件下该反应在达到最大限度 | |
| B. | t时刻表示该反应达到化学平衡状态 | |
| C. | t时刻以前正反应速率大于逆反应速率 | |
| D. | t时刻及以后正反应速率等于逆反应速率等于0 |
6.下列说法正确的是( )
| A. | 葡萄糖与果糖、淀粉与纤维素均互为同分异构体 | |
| B. | CH3-CH=CH-CH3与C3H6一定互为同系物 | |
| C. | 甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应 | |
| D. | C3H8的二氯代物共有3种 |


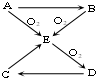 已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.