题目内容
8.0.1mol某有机物M在氧气中充分燃烧后,将产生的气体通过浓硫酸,浓硫酸增重7.2g,再将该气体通入500mL浓度为0.8mol/L NaOH溶液中,生成的两种钠盐Na2CO3与NaHCO3的物质的量之比为1:2,试计算(1)分别求出M中碳和氢的原子个数
(2)若M中只有一种官能团,且M能与Na反应放出氢气,试写出M的所有可能结构的结构简式.
分析 浓硫酸增重7.2g为H2O的质量,则n(H)=2×$\frac{7.2g}{18g/mol}$=0.8mol,所以分子中氢原子个数为$\frac{0.8mol}{0.1mol}$=8,再将该气体通入500mL浓度为0.8mol/L NaOH溶液中,生成的两种钠盐Na2CO3与NaHCO3的物质的量之比为1:2,设碳酸钠xmol,2x+2x=0.8×0.5,x=0.1,n(C)=0.3mol,所以分子中氢原子个数为:$\frac{0.3mol}{0.1mol}$=3,由此分析解答.
解答 解:浓硫酸增重7.2g为H2O的质量,则n(H)=2×$\frac{7.2g}{18g/mol}$=0.8mol,所以分子中氢原子个数为$\frac{0.8mol}{0.1mol}$=8,再将该气体通入500mL浓度为0.8mol/L NaOH溶液中,生成的两种钠盐Na2CO3与NaHCO3的物质的量之比为1:2,设碳酸钠xmol,2x+2x=0.8×0.5,x=0.1,n(C)=0.3mol,所以分子中氢原子个数为:$\frac{0.3mol}{0.1mol}$=3,(1)所以M中碳个数为3和氢的原子个数为8,答:碳个数为3和氢的原子个数为8;
(2)碳个数为3和氢的原子个数为8,说明分子中的氢已达饱,而且M能与Na反应放出氢气,说明M中含有醇羟基,可能是一元醇、二元醇或三元醇,可能结构简式为:CH3CH2CH2OH,(CH3)2CHOH,CH3CHOHCH2OH,HOCH2CH2CH2OH,HOCH2CHOHCH2OH,
答:CH3CH2CH2OH,(CH3)2CHOH,CH3CHOHCH2OH,HOCH2CH2CH2OH,HOCH2CHOHCH2OH.
点评 本题是考查有物分子式和结构简式的确定,注意燃烧法确定有机物的分子式中,元素守恒思想的应用,根据物质的性质结合分子式可书写结构简式,难度不大.

| A. | 150 mL 1 mol/L的NaCl溶液 | B. | 75 mL 2 mol/L的NH4Cl溶液 | ||
| C. | 150 mL 3 mol/L的KCl溶液 | D. | 75 mL 1 mol/L的BaCl2溶液 |
| A. | 胶体区别于其他分散系的本质特征是分散质微粒直径在10-9~10-7m之间 | |
| B. | 用平行光照射FeCl3溶液和Fe(OH)3胶体时,均能产生丁达尔现象 | |
| C. | 向豆浆中加入盐卤做豆腐是胶体聚沉在生活中的具体应用 | |
| D. | 溶液、胶体、浊液均属于混合物 |
| A. | ①② | B. | ②④ | C. | ②③④ | D. | ① |
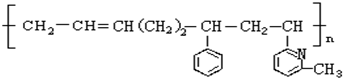
其单体可能是以下6种中的正确的组合是( )
①
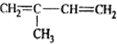 ②
②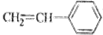 ③CH2=CH-CH=CH2④
③CH2=CH-CH=CH2④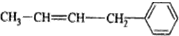 ⑤
⑤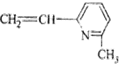 ⑥
⑥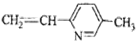
| A. | ②③⑤ | B. | ②③⑥ | C. | ①②⑥ | D. | ②④⑥ |
| A. | 丙烯 | B. | 苯 | C. | 甲苯 | D. | 乙炔 |
| A. | 大理石与稀盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 硫酸铜溶液与氢氧化钡溶液混合:Ba2++SO42-═BaSO4↓ | |
| C. | 将少量铜片放入浓硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | 向澄清石灰水中加入过量的小苏打溶液:OH-+HCO3-+Ca2+═CaCO3↓+H2O |
| A. | 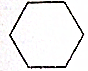 | B. |  | ||
| C. | 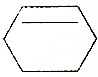 | D. |  |
 和
和 ⑧CH3CH2CH2CH3 和CH3CH2CH(CH3)2
⑧CH3CH2CH2CH3 和CH3CH2CH(CH3)2