题目内容
铝镁合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用于制作窗框、卷帘门等.下列性质与这些用途无关的是( )
| A、强度高 | B、不易生锈 |
| C、密度小 | D、导电、导热性好 |
考点:合金的概念及其重要应用
专题:
分析:铝镁合金具有耐腐蚀性、密度小、机械强度高等方面的特点,以此解答该题.
解答:
解:铝镁合金用于制作门窗、防护栏等时主要是利用了铝镁合金具有耐腐蚀性、密度小、机械强度高等方面的特点,与导电性是否良好无关.
故选:D.
故选:D.
点评:本题考查元素化合物知识,为高频考点,侧重于化学与生活的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意把握合金与金属单质的组成、性质以及用途的差异,难度不大.

练习册系列答案
相关题目
为了验证NaHCO3固体中是否含有Na2CO3,下列实验及判断中,正确的是( )
| A、加热,观察是否有气体放出 |
| B、溶于水后加石灰水,看有无沉淀 |
| C、溶于水后加MgCl2溶液,看有无沉淀 |
| D、加热后称量,看质量是否变化 |
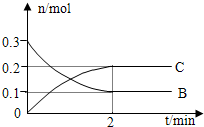 一定温度下,在2L的密闭容器中发生反应:A(g)+2B(g)?xC(g)△H<0,B、C的物质的量随时间变化的关系如图.下列有关说法不正确的是( )
一定温度下,在2L的密闭容器中发生反应:A(g)+2B(g)?xC(g)△H<0,B、C的物质的量随时间变化的关系如图.下列有关说法不正确的是( )| A、x=2 |
| B、2min后,降低温度平衡向右移动 |
| C、反应开始2min内ν(C)=0.1mol/(L?min) |
| D、当容器内混合气体压强不再改变时,反应体系达到化学平衡状态 |
下列物质反应后一定有+3价铁生成的是( )
①过量的Fe与Cl2反应;
②Fe与过量稀H2SO4反应后,再向其中加入KNO3;?
③Fe(NO3)2溶液中加入少量盐酸;?
④Fe和Fe2O3的混合物溶于盐酸中.
①过量的Fe与Cl2反应;
②Fe与过量稀H2SO4反应后,再向其中加入KNO3;?
③Fe(NO3)2溶液中加入少量盐酸;?
④Fe和Fe2O3的混合物溶于盐酸中.
| A、只有①?? |
| B、只有①②?? |
| C、只有①②③?? |
| D、全部 |
向某密闭容器中加入0.3molA,0.1molC和一定量的B三种气体在一定条件下发生反应,各物质浓度随时间变化如甲图所示[t0~tl阶段的c(B)变化未画出].乙图为t2时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件(浓度、温度、压强、催化剂)且互不相同,t3~t4阶段为使用催化剂.下列说法中正确的是( )
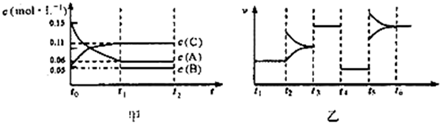

| A、其他条件不变时,增大压强,B的转化率不变 |
| B、t4~t5阶段改变的条件为降低温度 |
| C、B的起始物质的量为0.02mol |
| D、若t5~t6阶段改变的条件为升高温度,则正反应为吸热反应 |
2000年5月,保利集团在香港拍卖会上花费3000万港币购回了在八国联军入侵中国火烧圆明园上后流失的国宝,铜铸的牛首、猴首和虎首.普通的铜器在时间稍久时容易出现铜绿.这三件1760年铜铸的国宝240年后看上去仍然熠熠生辉.下面对其原因的分析中最可能的是( )
| A、它们的表面电镀上了一层耐磨的黄金 |
| B、环境污染日趋严重,它们表面的铜丝被酸雨溶解洗去 |
| C、铜的金属活动性比氢小,因此不易被氧化 |
| D、它们是含有一定比例的金、银、锡、锌的合金 |
关于电解质的下列说法中正确的是( )
| A、在水溶液中和熔化状态下能导电的化合物 |
| B、在水溶液中或熔化状态下能导电的物质 |
| C、在水溶液中或熔化状态下能导电的化合物 |
| D、在水溶液中或熔化状态下导电的离子由原物质本身电离出来的化合物 |