题目内容
下列物质反应后一定有+3价铁生成的是( )
①过量的Fe与Cl2反应;
②Fe与过量稀H2SO4反应后,再向其中加入KNO3;?
③Fe(NO3)2溶液中加入少量盐酸;?
④Fe和Fe2O3的混合物溶于盐酸中.
①过量的Fe与Cl2反应;
②Fe与过量稀H2SO4反应后,再向其中加入KNO3;?
③Fe(NO3)2溶液中加入少量盐酸;?
④Fe和Fe2O3的混合物溶于盐酸中.
| A、只有①?? |
| B、只有①②?? |
| C、只有①②③?? |
| D、全部 |
考点:铁的化学性质,铁的氧化物和氢氧化物,物质的检验和鉴别的基本方法选择及应用
专题:几种重要的金属及其化合物
分析:①氯气为强氧化剂,与变价金属反应生成高价金属化合物;
②稀硫酸为弱氧化剂,与Fe反应生成亚铁离子,但硝酸盐在酸性条件下具有强氧化性;
③硝酸盐在酸性条件下具有强氧化性;
④氧化铁与盐酸反应生成氯化铁,若Fe足量,发生Fe+2Fe3+=3Fe2+.
②稀硫酸为弱氧化剂,与Fe反应生成亚铁离子,但硝酸盐在酸性条件下具有强氧化性;
③硝酸盐在酸性条件下具有强氧化性;
④氧化铁与盐酸反应生成氯化铁,若Fe足量,发生Fe+2Fe3+=3Fe2+.
解答:
解:①过量的铁与氯气反应,生成氯化铁,与Fe的过量无关,故选;
②Fe与过量稀硫酸反应后,生成硫酸亚铁,再向其中加KNO3,发生氧化还原反应生成铁离子,故选;
③Fe(NO3)2溶液中加少量盐酸,发生发生氧化还原反应生成铁离子,故选;
④Fe和Fe2O3的混合物溶于盐酸中,若Fe足量,发生Fe+2Fe3+=3Fe2+,则不含铁离子,故不选;
故选C.
②Fe与过量稀硫酸反应后,生成硫酸亚铁,再向其中加KNO3,发生氧化还原反应生成铁离子,故选;
③Fe(NO3)2溶液中加少量盐酸,发生发生氧化还原反应生成铁离子,故选;
④Fe和Fe2O3的混合物溶于盐酸中,若Fe足量,发生Fe+2Fe3+=3Fe2+,则不含铁离子,故不选;
故选C.
点评:本题考查铁的化学性质及氧化还原反应,为高频考点,把握发生的氧化还原反应为解答的关键,注意氧化剂的氧化性及硝酸盐在酸性条件下的性质,题目难度不大.

练习册系列答案
相关题目
下列各组物质既不是同系物又不是同分异构体的是( )
| A、软脂酸和硬脂酸 |
| B、甲酸甲酯和乙酸 |
| C、油酸和乙酸 |
| D、对甲基苯酚和苯甲醇 |
A、B、C、D 4种化合物,其焰色反应均为浅紫色,A、B、C和盐酸反应都可得到D;B、C 以等物质的量在溶液中反应可得到A;若在B溶液中通入一种无色无刺激性气味的气体,适量时得A,过量时得C,则A、B、C、D分别是( )
| A、KHCO3 KAlO2 K2CO3 KCl |
| B、K2CO3 KOH KHCO3 KCl |
| C、K2SO4 KOH KHSO4 KCl |
| D、K2CO3 K2SiO3 KOH KCl |
铝镁合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用于制作窗框、卷帘门等.下列性质与这些用途无关的是( )
| A、强度高 | B、不易生锈 |
| C、密度小 | D、导电、导热性好 |
使石蕊试液变红的某透明溶液中,下列各组离子能大量共存的是( )
| A、CO32-、Na+、K+、OH- |
| B、Ba2+、CO32-、NO3-、SO42- |
| C、K+、Cu2+、Cl-、SO42- |
| D、Fe2+、NO3-、Cl-、SO42- |
①NaHCO3,②Al(OH)3 ③(NH4)2S ④SiO2 ⑤Al五种物质中,跟盐酸和氢氧化钠溶液都能反应的化合物是( )
| A、①②③⑤ | B、只有①②③ |
| C、只有①②③④ | D、全部 |
在用Zn、Cu片和CuSO4溶液组成的原电池装置中,经过一段时间工作后,下列说法中正确的是( )
| A、锌片是正极,铜片质量不变 |
| B、电流方向是从锌片流向铜片 |
| C、锌片是负极,铜片质量不变 |
| D、锌片是负极,铜片质量增加 |
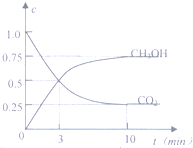 目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的客闭容器中,充入1molCO2和3molH2,在500℃下发生反应:CO2(g)+3H2O(g)?CH3OH(g)+H2O(g);
目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的客闭容器中,充入1molCO2和3molH2,在500℃下发生反应:CO2(g)+3H2O(g)?CH3OH(g)+H2O(g);