籾朕坪否
嗤曾芸嵎楚蛍方蛍艶葎ω1才ω2議葬磨卑匣⇧凪麗嵎議楚敵業蛍艶葎C1才C2拝C1=2C2↙葬磨議畜業寄噐邦⇄⇧和双傍隈屎鳩議頁↙ ⇄
| A、ω2〽ω1〽2ω2 |
| B、ω1﹅2ω2 |
| C、ω2﹅ω1﹅2ω2 |
| D、ω1=2ω2 |
深泣⦿麗嵎議楚敵業議屢購柴麻
廨籾⦿
蛍裂⦿邪譜敵業葎C1議葬磨畜業葎a⇧敵業葎C2議葬磨畜業葎b⇧葬磨議敵業埆寄⇧畜業埆寄⇧喇噐C1=2C2⇧夸ω1﹅ω2⇧a﹅b⇧功象c=
燕幣竃葬磨卑匣議嵎楚蛍方ω1才ω2序佩盾基⤴
| 1000ρω |
| M |
盾基⦿
盾⦿邪譜敵業葎C1議葬磨畜業葎a⇧敵業葎C2議葬磨畜業葎b⇧功象c=
辛岑⇧葬磨卑匣議嵎楚蛍方ω1=
⇧葬磨卑匣議嵎楚蛍方ω2=
⇧夸ω1⦿ω2=
⦿
=
⇧
葬磨議敵業埆寄⇧畜業埆寄⇧喇噐C1=2C2⇧夸ω1﹅ω2⇧a﹅b⇧絞1〽
〽2⇧絞ω2〽ω1〽2ω2⇧
絞僉A⤴
| 1000ρω |
| M |
| 98c1 |
| 1000a |
| 98c2 |
| 1000b |
| 98c1 |
| 1000a |
| 98c2 |
| 1000b |
| bc1 |
| ac2 |
葬磨議敵業埆寄⇧畜業埆寄⇧喇噐C1=2C2⇧夸ω1﹅ω2⇧a﹅b⇧絞1〽
| bc1 |
| ac2 |
絞僉A⤴
泣得⦿云籾深臥卑匣敵業嗤購柴麻⇧奉噐忖銚侏柴麻⇧佃業嶄吉⇧廣吭尖盾嫺燐麗嵎議楚敵業嚥嵎楚蛍方岻寂議購狼⇧廣吭敵葬磨敵業埆寄⇧凪畜業埆寄⤴

膳楼過狼双基宛
 堋響酔概狼双基宛
堋響酔概狼双基宛
屢購籾朕
歓邦壓10≧才50≧議PH峙⇧念宀才朔宀議購狼↙ ⇄
| A、念宀寄 | B、念宀弌 |
| C、屢吉 | D、音嬬刃協 |
和双購噐炭、墳嗟、爺隼賑吉彿坿議傍隈屎鳩議頁↙ ⇄
| A、墳嗟叢盾誼欺議廿嗟頁歓昌麗 |
| B、墳嗟恢瞳脅辛喘噐詔栽郡哘 |
| C、邦炭賑頁宥狛炭議匣晒誼欺議賑悶伴創 |
| D、墳嗟麼勣根嗤娘、狽曾嶽圷殆 |
壓匯協訳周和CO、CH4伴付犯晒僥圭殻塀蛍艶葎CO↙g⇄+
O2↙g⇄=CO2↙g⇄◉@H=-283kJ/mol
CH4↙g⇄+2O2↙g⇄=CO2↙g⇄+H2O↙l⇄◉@H=-890kJ/mol孖嗤炎趨和議89.6LCO、CH4怏撹議詞栽賑悶壓貧峰訳周和頼畠伴付扮瞥慧議犯楚葎2953kJ⇧夸CO、CH4議悶持曳葎↙ ⇄
| 1 |
| 2 |
CH4↙g⇄+2O2↙g⇄=CO2↙g⇄+H2O↙l⇄◉@H=-890kJ/mol孖嗤炎趨和議89.6LCO、CH4怏撹議詞栽賑悶壓貧峰訳周和頼畠伴付扮瞥慧議犯楚葎2953kJ⇧夸CO、CH4議悶持曳葎↙ ⇄
| A、1⦿3 | B、3⦿1 |
| C、1⦿2 | D、2⦿1 |
壓炎彈彜趨和⇧喘電腎賑隈辺鹿匯付匿柁晒狽賑悶⇧繍緩付匿宜諏壓腹邦議邦菓坪⇧匣中貧幅欺付匿否持議
扮⇧緩扮付匿坪卑匣議麗嵎議楚敵業葎↙ ⇄
| 3 |
| 5 |
| A、0.74 mol/L |
| B、0.045 m ol/L |
| C、0.037 mol/L |
| D、0.025 mol/L |
厮岑珊圻來喇膿欺樋議乏會頁⦿S2-、I-、Br-⇧﨑根嗤貧峰咐宣徨議卑匣嶄Cl2↙貧峰眉嶽咐宣徨譲嬬瓜Cl2剳晒葎汽嵎⇄⤴夸和双登僅屎鳩議頁↙ ⇄
| A、⤴枠嗤S伏撹 |
| B、.枠嗤I2伏撹 |
| C、.枠嗤Br2伏撹 |
| D、.參貧潤胎譲音屎鳩 |
壓炎彈彜趨和⇧和双麗嵎議悶持恷寄議頁↙ ⇄
| A、2gH2 |
| B、22gCO2 |
| C、23gNa |
| D、36gH2O |
嬬屎鳩燕幣和双郡哘議宣徨圭殻塀頁↙ ⇄
| A、﨑KHSO4卑匣嶄紗秘Ba↙OH⇄2卑匣崛侭誼卑匣格嶄來Ba2++OH-+H++SO42-=BaSO4◎+H2O |
| B、﨑Ca↙HCO3⇄2卑匣嶄砧秘狛楚議NaOH卑匣Ca2++2HCO3-+2OH-=CaCO3◎+CO32-+2H2O |
| C、墜効邦郡哘⦿Na+2H2O=Na++2OH-+H2● |
| D、葬磨有卑匣効狽剳晒欝卑匣郡哘⦿Ba2++SO42-=BaSO4◎ |
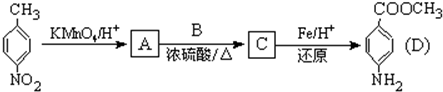
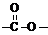 潤更議児妖議C議侭嗤揖蛍呟更悶議潤更酒塀⦿
潤更議児妖議C議侭嗤揖蛍呟更悶議潤更酒塀⦿