题目内容
16.下列物质中,既含共价键又含离子键的是( )| A. | KCl | B. | H2O | C. | Na2O2 | D. | CO2 |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,第IA、IIA族元素和第VIA、VIIA族元素之间易形成离子键.
解答 解:A.KCl中钾离子和氯离子之间只存在离子键,故A错误;
B.H2O分子中H原子和O原子之间只存在共价键,故B错误;
C.Na2O2中钠离子和过氧根离子之间存在离子键、O原子和O原子之间存在共价键,故C正确;
D.二氧化碳只存在共价键,故D错误;
故选C.
点评 本题考查了离子键和共价键的判断,根据共价键和离子键的形成原因来分析解答,易错选项是C,注意氯化钙中两个氯离子之间不存在化学键,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列图示与对应的叙述符合的是( )
| A. | 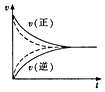 用实线、虚线分别表示某可逆反应未使用催化剂和使用催化剂的正、逆反应速率随时间的变化 | |
| B. | 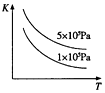 表示反应2SO2(g)+O2(g)?2SO3(g)△H<0的平衡常数K与温度和压强的关系 | |
| C. | 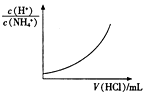 表示向0.1mol/L的NH4Cl溶液中滴加0.1mol/L的HCl溶液时,溶液中$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$随HCl溶液体积变化关系 | |
| D. | 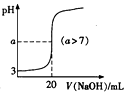 表示常温下向20mL pH=3的醋酸中滴加pH=11的NaOH溶液,溶液的pH随NaOH溶液体积的变化关系 |
4.现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(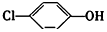 ),同时利用此装置的电能在铁上,下列说法正确的是( )
),同时利用此装置的电能在铁上,下列说法正确的是( )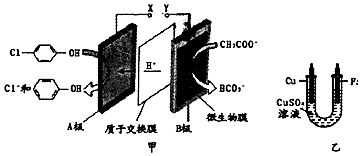
 ),同时利用此装置的电能在铁上,下列说法正确的是( )
),同时利用此装置的电能在铁上,下列说法正确的是( )
| A. | 当外电路中有0.2mol e-转移时,A极区增加的H+的个数为0.2 NA | |
| B. | A极的电极反应式为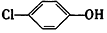 +2e-+H+=Cl-+ +2e-+H+=Cl-+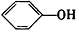 | |
| C. | 乙装置中铁电极应与甲装置中X相连接 | |
| D. | 电镀过程中乙装置中CuSO4溶液浓度逐渐减小 |
11.下列元素中,属于主族元素的是( )
| A. | Cu | B. | Na | C. | Fe | D. | Zn |
1.依据元素周期表判断,下列各组关系中正确的是( )
| A. | 稳定性:NH3>H2O>H2S | B. | 氧化性:Cl2>S>P | ||
| C. | 酸性:H3PO4>H2SO4>HClO4 | D. | 碱性:Mg(OH)2>Ca(OH)2>Ba(OH)2 |
5.“银针验毒”在我国有上千年历史,银针主要用于检验是否有含硫元素的有毒物质.其反应原理之一为:Ag+2H2S+O2→Ag2S+H2O.当银针变色后,将其置于盛有食盐水的铝制容器中一段时间后便可复原.以下说法不正确的是( )
| A. | 当银针变黑时,所检验的物质有毒 | |
| B. | 银针验毒时,Ag被氧化 | |
| C. | 上述验毒反应的氧化产物和还原产物的物质的量之比为1:1 | |
| D. | 银针复原发生的反应可能为:3Ag2S+2Al═6Ag+Al2S3 |
6.下列指定反应的离子方程式正确的是( )
| A. | 向碳酸钠溶液中加入过量醋酸:CO32-+2H+═H2O+CO2↑ | |
| B. | 向偏铝酸钠溶掖中通入过量二氧化碳;CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- | |
| C. | 向莫尔盐[(NH4)2Fe(SO4)2•6H2O]溶液中加入过量氧氧化钠溶液:NH4++Fe2++3OH-═NH3•H2O+Fe(OH)2↓ | |
| D. | 向双氧水中加入酸性高锰酸钾溶液:5H2O2+2MnO4-═2Mn2++5O2↑+6OH-+2H2O |



