题目内容
5.“银针验毒”在我国有上千年历史,银针主要用于检验是否有含硫元素的有毒物质.其反应原理之一为:Ag+2H2S+O2→Ag2S+H2O.当银针变色后,将其置于盛有食盐水的铝制容器中一段时间后便可复原.以下说法不正确的是( )| A. | 当银针变黑时,所检验的物质有毒 | |
| B. | 银针验毒时,Ag被氧化 | |
| C. | 上述验毒反应的氧化产物和还原产物的物质的量之比为1:1 | |
| D. | 银针复原发生的反应可能为:3Ag2S+2Al═6Ag+Al2S3 |
分析 Ag+2H2S+O2→Ag2S+H2O反应中黑色物质为Ag2S,Ag在反应中化合价升高,为还原剂,氧气在反应中化合价降低,为氧化剂,生成的Ag2S是氧化产物,H2O为还原产物,银针变色后,将其置于盛有食盐水的铝制容器中一段时间后便可复原,发生原电池反应,硫化银被还原生成银,以此解答该题.
解答 解:A.当银针变黑时,说明生成Ag2S,可说明所检验的物质有毒,故A正确;
B.反应生成硫化银,Ag元素化合价升高,被氧化,故B正确;
C.反应的方程式为4Ag+2H2S+O2═2Ag2S+2H2O,生成的Ag2S是氧化产物,H2O为还原产物,则氧化产物和还原产物的物质的量之比为1:1,故C正确;
D.形成原电池反应时,负极反应式为Al-3e-+3H2O=Al(OH)3+3H+,正极反应式为3Ag2S+6H++6e-═6Ag+3H2S↑,总方程式为2Al+3Ag2S+6H2O=6Ag+3H2S↑+2Al(OH)3,故D错误.
故选D.
点评 本题考查氧化还原反应,为高频考点,侧重考查学生的分析能力,题目难度不大,注意从化合价变化的角度判断,注意该反应中S元素的化合价没有变化,把握原电池的工作原理.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.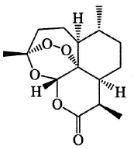 中国药学家屠呦呦因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖.青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )
中国药学家屠呦呦因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖.青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )
 中国药学家屠呦呦因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖.青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )
中国药学家屠呦呦因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖.青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )| A. | 提取过程中为防止破坏青蒿素结构,应避免高温,故采用低沸点溶剂乙醚进行萃取 | |
| B. | 可使用质谱仪测出这个分子的相对分子质量,也可用紫外光谱确定这个分子的环状结构 | |
| C. | 青蒿素是脂溶性的,既可看作是醚类也可看作是酯类,既有氧化性又有还原性 | |
| D. | 元素分析仪可以确定青蒿素中是否含有C、H、O等元素 |
16.下列物质中,既含共价键又含离子键的是( )
| A. | KCl | B. | H2O | C. | Na2O2 | D. | CO2 |
13.下列实验中.对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验步骤 | 现象 | 结论 |
| A | 向KI溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 碘易溶于CCl4,难溶于水 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 产生白色沉淀,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | FeCl3和BaCl2混合溶液中通入足量SO2 | 溶液变为浅绿色且有白色沉淀生成 | 沉淀为BaSO3 |
| D | 向AgCl悬浊液中加入NaI溶液 | 出现黄色沉淀 | Ksp (AgCl)<Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
20.根据下列实验操作和实验现象所得结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向石蕊溶液中滴加氯水至足量 | 石蕊溶液先变红再褪色 | Cl2有酸性和漂白性 |
| B | 向大豆油、煤油中分别加入足量NaOH溶液,充分加热 | 一种液体仍然分层,另一种液体不再分层 | 分层者为煤油,不分层者为大豆油 |
| C | 向某溶液中加入足量盐酸 | 生成白色沉淀 | 该溶液中含有Ag+ |
| D | 用容量瓶配制一定物质的量浓度的K2SO4溶液,定容后反复摇匀 | 液面低于刻度线 | 所配溶液浓度偏高 |
| A. | A | B. | B | C. | C | D. | D |
10.化学与生产、生活、科技、环境等密切相关,下列说法正确的是( )
| A. | 研发使用高效催化剂,可提高反应中原料的转化率 | |
| B. | 铅笔芯的原材料为铅,所以儿童常咬铅笔头容易铅中毒 | |
| C. | 网络飞速发展,得益于光纤良好的导电性,光纤的主要成分是二氧化硅 | |
| D. | 用K2FeO4取代Cl2处理饮用水,不仅可杀菌消毒,同时还能沉降水中的悬浮物 |
17.工业上可由乙苯(C8H10)生产苯乙烯(C8H8),其反应原理是: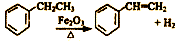 下列说法中错误的是( )
下列说法中错误的是( )
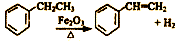 下列说法中错误的是( )
下列说法中错误的是( )| A. | 可用溴的四氯化碳来鉴别乙苯和苯乙烯 | |
| B. | 乙苯分子中所有原子可能都处于同一平面 | |
| C. | 苯乙烯可发生氧化反应、取代反应、加成反应 | |
| D. | 乙苯与苯互为同系物 |
14.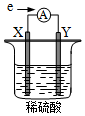 在盛有稀 H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.关于该装置,下列说法正确的是( )
在盛有稀 H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.关于该装置,下列说法正确的是( )
 在盛有稀 H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.关于该装置,下列说法正确的是( )
在盛有稀 H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.关于该装置,下列说法正确的是( )| A. | 外电路中电流方向为:X→ →Y →Y | |
| B. | 若两电极分别为铁棒和碳棒,则 X 为碳棒,Y 为铁棒 | |
| C. | X 极上发生的是还原反应,Y 极上发生的是氧化反应 | |
| D. | 若两电极都是金属单质,则它们的活动性顺序为 X>Y |
15.利用下列实验装置能完成相应实验的是( )
| A. | 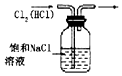 除去Cl2中的HCl | B. | 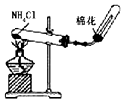 实验室制氨气 | ||
| C. | 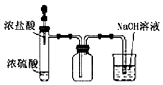 制取并收集HCl | D. |  证明乙醇发生消去反应生成了乙烯 |