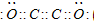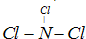��Ŀ����
����A��B��C��D��E����ǿ����ʣ�������ˮ�пɵ��������������(�������Ӳ��ظ�)�������� | H+��Na+��Al3+��Ag+��Ba2+ |
������ | OH-��Cl-�� |
��֪����A��B����Һ�ʼ��ԣ�C��D��E��Һ�����ԡ���A��Һ��E��Һ��Ӧ�����������г���������A��Һ��C��Һ��Ӧֻ���������(�������������ͬ)����D��Һ������������Һ��Ӧ���ܲ���������Cֻ����D��Ӧ����������
�Իش��������⣺
(1)��C��Һ��μ��������������ʵ���Ũ�ȵ�A��Һ�У���Ӧ����Һ�и�������Ũ���ɴ�С��˳��Ϊ��____________��
(2)д��E��Һ�������B��Һ��Ӧ�����ӷ���ʽ��__________________________��
(3)��֪��NaOH(aq)+HNO3(aq)![]() NaNO3(aq)+H2O(l)����H=-akJ��mol-1����д��B��C��ϡ��Һ��Ӧ���Ȼ�ѧ����ʽ��____________________________________________________��
NaNO3(aq)+H2O(l)����H=-akJ��mol-1����д��B��C��ϡ��Һ��Ӧ���Ȼ�ѧ����ʽ��____________________________________________________��
(4)��100 mL0.1 mol��L-1E��Һ�У���μ���35mL2mol��L-1 NaOH��Һ�����յõ����������ʵ���Ϊ__________________��
(1)c(Na+)��c(Cl-)��c(![]() )��c(OH-)��c(H+)��c(
)��c(OH-)��c(H+)��c(![]() )
)
��c(Na+)��c(Cl-)��c(![]() )��c(OH-)��c(H+)
)��c(OH-)��c(H+)
(2)2Al3++3![]() +3Ba2++8OH-
+3Ba2++8OH-![]() 2
2![]() +3BaSO4��+4H2O
+3BaSO4��+4H2O
(3)OH-(aq)+H+(aq)![]() H2O(l)����H=-a kJ��mol
H2O(l)����H=-a kJ��mol
��![]() Ba(OH)2(aq)+HCl(aq)
Ba(OH)2(aq)+HCl(aq)![]()
![]() BaCl2(aq)+H2O(l)����H=-akJ��mol
BaCl2(aq)+H2O(l)����H=-akJ��mol
��Ba(OH)2(aq)+2HCl(aq)![]() BaCl2(aq)+2H2O(l)����H=-2akJ��mol
BaCl2(aq)+2H2O(l)����H=-2akJ��mol
(4)0.01 mol��

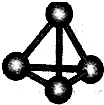 ����A��B��C��D��E��F���ֶ�����Ԫ�أ����ǵ�ԭ��������������D��E���⻯����ӹ��Ͷ���V�ͣ�A��B������������֮����C��������������ȣ�A�ֱܷ���B��C��D�γɵ���������ȵķ��ӣ���A��D���γɵĻ���������¾�ΪҺ̬��
����A��B��C��D��E��F���ֶ�����Ԫ�أ����ǵ�ԭ��������������D��E���⻯����ӹ��Ͷ���V�ͣ�A��B������������֮����C��������������ȣ�A�ֱܷ���B��C��D�γɵ���������ȵķ��ӣ���A��D���γɵĻ���������¾�ΪҺ̬��