题目内容
2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭.“亮菌甲素”的结构简式为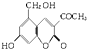 ,它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.请回答下列问题:
,它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.请回答下列问题:
(1)丙二醇的分子式是C3H8O2,已知两个羟基连在同一个碳原子上的物质不存在.写出其属于醇类的同分异构体的结构简式 .
(2)下列有关“亮菌甲素”的叙述正确的是 (填字母).
A.“亮菌甲素”能与H2发生加成反应
B.不能使酸性KMnO4溶液褪色
C.“亮菌甲素”分子中含氧官能团只有2种
D.1mol“亮菌甲素”最多与2molNaOH反应
(3)核磁共振仪可以测定有机物分子中处于不同化学环境的氢原子及相对数量.氢原子在分子中的化学环境不同,在核磁谱图中就处于不同的位置,化学环境相同的氢原子越多,波谱峰积分面积越大(或高度越高).核磁共振氢谱分析,发现二甘醇分子中有3个吸收峰,其峰面积之比为2:2:1.又知二甘醇中C、O元素的质量分数相同,且H的质量分数为9.4%,1mol二甘醇与足量金属钠反应生成1mol H2.写出二甘醇的结构简式 ,二甘醇与乙酸(按物质的量之比1:1)反应的化学方程式 .
 ,它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.请回答下列问题:
,它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.请回答下列问题:(1)丙二醇的分子式是C3H8O2,已知两个羟基连在同一个碳原子上的物质不存在.写出其属于醇类的同分异构体的结构简式
(2)下列有关“亮菌甲素”的叙述正确的是
A.“亮菌甲素”能与H2发生加成反应
B.不能使酸性KMnO4溶液褪色
C.“亮菌甲素”分子中含氧官能团只有2种
D.1mol“亮菌甲素”最多与2molNaOH反应
(3)核磁共振仪可以测定有机物分子中处于不同化学环境的氢原子及相对数量.氢原子在分子中的化学环境不同,在核磁谱图中就处于不同的位置,化学环境相同的氢原子越多,波谱峰积分面积越大(或高度越高).核磁共振氢谱分析,发现二甘醇分子中有3个吸收峰,其峰面积之比为2:2:1.又知二甘醇中C、O元素的质量分数相同,且H的质量分数为9.4%,1mol二甘醇与足量金属钠反应生成1mol H2.写出二甘醇的结构简式
考点:有机物的推断,有机物实验式和分子式的确定,有机物的结构和性质,同分异构现象和同分异构体
专题:
分析:(1)两个羟基在不同的碳原子上,有相邻和相间两种位置;
(2)“亮菌甲素”中含有酚羟基、醇羟基、醚键以及酯基等官能团;
(3)根据元素的含量判断分子式,二甘醇分子中有3个吸收峰,其峰面积之比为2:2:1,说明分子中有3种不同的H,且个数比为2:2;1,1mol二甘醇与足量的金属钠反应生成1molH2,说明含有2个-OH,以此解答该题.
(2)“亮菌甲素”中含有酚羟基、醇羟基、醚键以及酯基等官能团;
(3)根据元素的含量判断分子式,二甘醇分子中有3个吸收峰,其峰面积之比为2:2:1,说明分子中有3种不同的H,且个数比为2:2;1,1mol二甘醇与足量的金属钠反应生成1molH2,说明含有2个-OH,以此解答该题.
解答:
解:(1)丙二醇的分子式是C3H8O2,对应的同分异构体中两个羟基在不同的碳原子上,有相邻和相间两种位置,为HOCH2CH2CH2OH、CH3CHOHCHOH,
故答案为:HOCH2CH2CH2OH、CH3CHOHCHOH;
(2)A.“亮菌甲素”中含有苯环和C=C键,能与H2发生加成反应,故A正确;
B.“亮菌甲素”中含有酚羟基和醇羟基,二者都能使酸性KMnO4退色,故B错误;
C.“亮菌甲素”中含有酚羟基、醇羟基、醚键以及酯基等官能团,含氧官能团有4种,故C错误;
D.“亮菌甲素”中含有酚羟基,具有酸性,含有酯基,可在碱性条件下水解,可以与NaOH反应,且-COOC水解后生成的酚-OH也反应,共消耗3molNaOH,故D错误.
故答案为:A;
(3)二甘醇中C、O元素的质量分数相同,且H的质量分数为9.4%,则C、O元素的质量分数都为
=45.3%,则分子中N(C):N(H):N(O)=
:
:
=4:3:10,分子式应为C4H10O3,
二甘醇分子中有3个吸收峰,其峰面积之比为2:2:1,说明分子中有3种不同的H,且个数比为2:2;1,1mol二甘醇与足量的金属钠反应生成1molH2,说明含有2个-OH,则二甘醇结构简式为HOCH2CH2OCH2CH2OH,与乙酸发生酯化反应为HOCH2CH2OCH2CH2OH+CH3COOH
HOCH2CH2OCH2CH2OOCCH3+H2O,
故答案为:HOCH2CH2OCH2CH2OH;HOCH2CH2OCH2CH2OH+CH3COOH
HOCH2CH2OCH2CH2OOCCH3+H2O.
故答案为:HOCH2CH2CH2OH、CH3CHOHCHOH;
(2)A.“亮菌甲素”中含有苯环和C=C键,能与H2发生加成反应,故A正确;
B.“亮菌甲素”中含有酚羟基和醇羟基,二者都能使酸性KMnO4退色,故B错误;
C.“亮菌甲素”中含有酚羟基、醇羟基、醚键以及酯基等官能团,含氧官能团有4种,故C错误;
D.“亮菌甲素”中含有酚羟基,具有酸性,含有酯基,可在碱性条件下水解,可以与NaOH反应,且-COOC水解后生成的酚-OH也反应,共消耗3molNaOH,故D错误.
故答案为:A;
(3)二甘醇中C、O元素的质量分数相同,且H的质量分数为9.4%,则C、O元素的质量分数都为
| 1-9.4% |
| 2 |
| 0.453 |
| 12 |
| 0.453 |
| 16 |
| 0.094 |
| 1 |
二甘醇分子中有3个吸收峰,其峰面积之比为2:2:1,说明分子中有3种不同的H,且个数比为2:2;1,1mol二甘醇与足量的金属钠反应生成1molH2,说明含有2个-OH,则二甘醇结构简式为HOCH2CH2OCH2CH2OH,与乙酸发生酯化反应为HOCH2CH2OCH2CH2OH+CH3COOH
| 浓H2SO4 |
| △ |
故答案为:HOCH2CH2OCH2CH2OH;HOCH2CH2OCH2CH2OH+CH3COOH
| 浓H2SO4 |
| △ |
点评:本题考查有机物的推断,题目难度中等,易错点为(3),注意分子式的推断为解答该题的关键,结合题目信息分析可能具有的结构.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
下列说法不正确的是( )
| A、做“食醋总酸含量的测定”实验时,必须先将市售食醋稀释10倍,然后用洗净的酸式滴定管量取一定体积的稀释液于洁净的锥形瓶中,锥形瓶不需要先用醋酸溶液润洗 |
| B、培养明矾晶体时,为得到较大颗粒的晶体,应自然冷却,并静置过夜 |
| C、铁钉镀锌前,先要用砂纸打磨直至表面变得光滑,然后放入氢氧化钠溶液中浸泡5分钟,用水洗净后还需放入稀盐酸中浸泡,再用水洗净 |
| D、制摩尔盐时用酒精洗涤产品,制阿司匹林时用冷水洗涤产品 |
两种气态烃以任意比例混合,在105℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L.下列各组混合烃中不符合此条件的是( )
| A、CH4与C2H4 |
| B、C2H2与C3H6 |
| C、C2H4与C3H4 |
| D、CH4与C3H4 |
已知下列热化学方程式,且b>a.Hg(l)+
O2(g)=HgO(s)△H=-a kJ?mol-1Zn(s)+
O2(g)=ZnO(s)△H=-b kJ?mol-1由此可知反应Zn(s)+HgO(s)=ZnO(s)+Hg(l)的焓变为( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、-(b-a) kJ?mol-1 |
| B、+(b-a) kJ?mol-1 |
| C、(b-a) kJ?mol-1 |
| D、(b+a) kJ?mol-1 |