题目内容
【题目】一种利用生物电化学方法脱除水体中NH4+的原理如图所示。
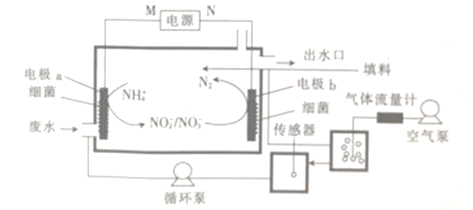
下列说法正确的是
A. M为电源的负极,N为电源的正极
B. 装置工作时,电极a周围溶液的pH降低
C. 装置内工作温度越高,NH4+的脱除率一定越大
D. 电极b上发生的反应之一为2NO2-+8H++8e-=N2↑+4H2O
【答案】B
【解析】A.电极a上NH4+失电子反应生成NO2-,电极a为阳极,所以M为电源的正极,N为电源的负极,故A错误;B.电极a上的反应为NH4+-6e-+2H2O= NO2-+8H+或者NH4+-8e-+3H2O= NO3-+10H+电极a周围溶液的pH降低,故B正确;C.细菌需要在正常温度范围内才能有效工作,温度太高容会使细菌死亡,故C错误;D.电极B上反应之一应该是2NO2-+8H++6e-=N2↑+4H2O,故D错误;本题选B。

【题目】根据下列实验操作、现象,所得结论正确的是
实验操作 | 实验现象 | 实验结论 | |
A | 在盛番茄汤的玻璃杯中加入适量植物油,充分搅拌、静置 | 上层液体颜色比下层液体深 | 番茄色素在水中的溶解度比在植物油中的大 |
B | 向Na2SiO3溶液中加入1~2滴酚酞溶液,再逐渐滴入稀盐酸,边加边振荡 | 溶液红色变浅并接近消失时,有透明的凝胶产生 | 制得了硅酸胶体 |
C | 向盛有10mL水的锥形瓶中,小心滴入SOCl2液体 | 剧烈反应,液面有白雾形成,并有带刺激性气味的气体逸出,该气体能使品红溶液褪色 | SOCl2与水发生了氧化还原反应 |
D | 向滴有酚酞溶液的碳酸钠溶液中滴加足量氯化钡溶液 | 析出白色沉淀,溶液红色褪去 | 氯化钡溶液显酸性 |
A. A B. B C. C D. D
【题目】a、b、c、d、e、f、g为七种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下所示:(单位:电荷)
粒子代号 | a | b | c | d | e | f | g |
原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
电荷数 | |||||||
(单位电荷) | 0 | +1 | -1 | 0 | +2 | +1 | 0 |
其中b的离子半径大于e的离子半径;c与f可形成两个共价型g分子。
试写出:
(1)a粒子的原子结构示意图是________;b粒子的电子排布式为________。
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为________(用化学式表示)。
(3)若d极易溶于水,在水溶液中变化的方程式为________,d分子的空间构型为________,键角为________;若d为正四面体形分子,其电子式为________。
(4)c粒子是________,f粒子是________(用化学式表示),由c、f生成g的离子方程式是________。



