题目内容
下列实验操作中错误的是( )
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口附近 |
| C、蒸发结晶时,要用玻璃棒不断搅拌,直至溶液蒸干,停止加热 |
| D、称量NaOH固体时,药品放在烧杯中置于托盘天平左盘,砝码放在右盘 |
考点:物质的分离、提纯的基本方法选择与应用,计量仪器及使用方法
专题:实验设计题
分析:A.分液时,应避免液体重新混合而污染;
B.蒸馏时,温度计用于测量馏分的温度;
C.蒸发时,应防止温度过高而导致固体分解而变质;
D.称量时,应避免氢氧化钠潮解、变质.
B.蒸馏时,温度计用于测量馏分的温度;
C.蒸发时,应防止温度过高而导致固体分解而变质;
D.称量时,应避免氢氧化钠潮解、变质.
解答:
解:A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出,目的是防止液体重新混合而污染,故A正确;
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口,用于测量馏分的温度,故B正确;
C.蒸发时,当有大量固体析出时应停止加热,用余热蒸干,目的是防止温度过高而导致固体分解而变质,故C错误;
D.氢氧化钠易潮解,且易与空气中二氧化碳反应,称量时,应放在小烧杯中称量,故D正确.
故选C.
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口,用于测量馏分的温度,故B正确;
C.蒸发时,当有大量固体析出时应停止加热,用余热蒸干,目的是防止温度过高而导致固体分解而变质,故C错误;
D.氢氧化钠易潮解,且易与空气中二氧化碳反应,称量时,应放在小烧杯中称量,故D正确.
故选C.
点评:本题考查物质的分离、提纯等基本操作,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验注意事项和操作方法,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
R元素的原子,其最外层电子数是次外层的电子数的2倍,则R是( )
| A、S | B、Si | C、Na | D、C |
常温下pH=3的盐酸与pH=9的NaOH溶液等体积混合(假设体积等于混合前两溶液体积和),混合溶液中c(H+)的计算式是( )
A、
| ||
B、
| ||
C、
| ||
| D、以上计算式都不对 |
用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、1 mol NH3中含有中子数为7NA个 |
| B、标准状况下,11.2 L H2O含有的分子数为0.5NA |
| C、2g氢气所含质子数是NA |
| D、由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
加热N2O5时,发生以下两个反应:N2O5?N2O3+O2,N2O3?N2O+O2.在1L密闭容器中加热4molN2O5,达到平衡时,c(O2)为4.5mol/L,c(N2O3) 为1.62mol/L,则c(N2O5) 为( )
| A、1.44mol/L |
| B、3.48mol/L |
| C、0.94mol/L |
| D、1.98mol/L |
下列化学式中只能表示一种物质的是( )
| A、C3H7OH |
| B、CH2O2 |
| C、C4H6 |
| D、C3H6O2 |
纯水在25℃时的氢离子浓度与90℃时的氢离子浓度的关系是( )
| A、大于 | B、等于 |
| C、小于 | D、不能肯定 |
下列离子在溶液中能够共存并且在加入少量的Na2O2固体后原离子浓度能基本保持不变的是( )
| A、NH4+、Ba2+、Cl-、NO3- |
| B、K+、AlO2-、Cl-、SO42- |
| C、Ca2+、Mg2+、NO3-、HCO3- |
| D、Na+、Cl-、HSO3-、NO3- |
某有机物的结构简式为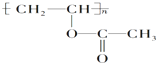 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )
 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )| A、1mol该有机物与NaOH溶液完全反应时,消耗NaOH 1mol |
| B、该有机物水解所得产物能发生取代反应 |
| C、该有机物可通过加聚反应生成 |
| D、该有机物的单体只有一种且能使溴水褪色 |