题目内容
16.关于NaHCO3 的性质,下列说法中正确的是( )| A. | 相同温度下溶解度比碳酸钠要大 | |
| B. | 热稳定性比碳酸钠要差 | |
| C. | 只能和酸反应不能和碱反应 | |
| D. | 和酸反应放出等量的二氧化碳,所消耗的酸比碳酸钠多 |
分析 A.碳酸钠的溶解度大于碳酸氢钠;
B.碳酸氢钠加热分解生成碳酸钠、二氧化碳气体和水,而碳酸钠加热不分解;
C.碳酸氢钠能够与酸反应生成二氧化碳气体,还能够与碱溶液发生中和反应;
D.根据碳酸钠、碳酸氢钠与酸反应的关系式分析.
解答 解:A.相同温度下,碳酸钠的溶解度比碳酸氢钠大,故A错误;
B.碳酸氢钠加热发生反应2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,而碳酸钠加热不分解,则热稳定性碳酸氢钠比碳酸钠差,故B正确;
C.碳酸氢钠能够与酸反应生成生成二氧化碳,也能够与碱溶液发生中和反应,故C错误;
D.碳酸钠、碳酸氢钠与氢离子反应关系式为:Na2CO3~2H+、NaHCO3~H+,生成等量的二氧化碳时,消耗碳酸钠、碳酸氢钠的物质的量相等,根据关系式可知碳酸钠消耗的酸多,故D错误;
故选B.
点评 本题考查了碳酸钠、碳酸氢钠的性质,题目难度不大,明确钠的化合物组成及性质为解答关键,注意掌握碳酸钠、碳酸氢钠的性质,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
6.下列变化属于吸热反应的是( )
| A. | 氯酸钾分解制氧气 | B. | 生石灰与水反应生成熟石灰 | ||
| C. | Ba(OH)2•8H2O与NH4Cl反应 | D. | 液态水汽化 |
7.下列物质中,属于强电解质的是( )
| A. | 铜 | B. | Na2SO4 | C. | CH3COOH | D. | NaCl 溶液 |
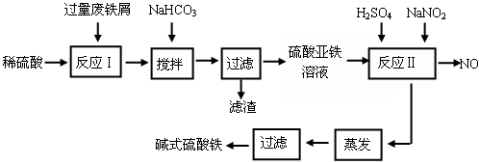
4.碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH在4.4-7.5范围内,使溶液中的杂质离子沉淀.该工艺中“搅拌”的作用是增大接触面积、加快反应速率.
(2)反应Ⅱ中加入NaNO2的目的是氧化Fe2+,发生反应的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,Fe(OH)2+可部分水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-.为检验所得产品中是否含有Fe2+,应使用的试剂为D
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液.

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)加入少量NaHCO3的目的是调节pH在4.4-7.5范围内,使溶液中的杂质离子沉淀.该工艺中“搅拌”的作用是增大接触面积、加快反应速率.
(2)反应Ⅱ中加入NaNO2的目的是氧化Fe2+,发生反应的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,Fe(OH)2+可部分水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-.为检验所得产品中是否含有Fe2+,应使用的试剂为D
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液.
11.H+浓度相同的两份等体积溶液A和B,A为HCl溶液,B为CH3COOH溶液,二者分别和等质量的锌反应,若最后仅有一份溶液中存在锌,则下列说法正确的是( )
①开始时的反应速率:A>B ②参加反应的锌的物质的量:A=B
③反应过程的平均速率:B>A ④A中有锌剩余 ⑤B中有锌剩余.
①开始时的反应速率:A>B ②参加反应的锌的物质的量:A=B
③反应过程的平均速率:B>A ④A中有锌剩余 ⑤B中有锌剩余.
| A. | ③④ | B. | ③⑤ | C. | ①③④ | D. | ①②③ |
1.相同物质的量的Na2CO3和NaHCO3固体都经过充分加热后的固体分别跟足量的盐酸反应.下列判断正确的是( )
| A. | 消耗盐酸一样多 | B. | 放出CO2一样多 | ||
| C. | 消耗盐酸后者多 | D. | 后者放出CO2的量是前者的一半 |
8.下列化工生产过程中所发生的主要化学反应不属于氧化还原反应的是( )
| A. | 用氯气和消石灰制漂白粉 | B. | 铝热法冶炼金属铁 | ||
| C. | 用油脂制肥皂 | D. | 电解水制H2 |
6.物质P(结构见图)是近期微博热传的“苯宝宝表情包”中的一种.物质P属于( )
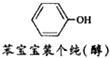

| A. | 碱 | B. | 烃 | C. | 无机物 | D. | 有机物 |
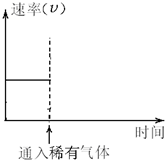 已知一定温度和压强下,在起始容积为V L的容器中充入1mol A和1mol B,保持恒温恒压下反应:A(g)+B(g)?C(g)△H>0.达到平衡时,C的体积分数为40%.试回答:
已知一定温度和压强下,在起始容积为V L的容器中充入1mol A和1mol B,保持恒温恒压下反应:A(g)+B(g)?C(g)△H>0.达到平衡时,C的体积分数为40%.试回答: