题目内容
以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等。实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如下:
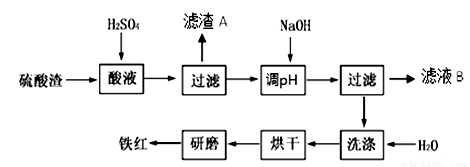
(1)硫酸渣的成分中属于两性氧化物的是 , 写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式: ;
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是_________;(部分阳离子以氢氧化物形式沉淀时溶液的pH见下表)
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(3)滤渣A的主要成分为 ,滤液B可以回收的物质有Na2SO4、MgSO4和___________;
(4)已知硫酸渣质量为w kg,假设铁红制备过程中,铁元素损耗25%,最终得到铁红的质量为m kg,则原来硫酸渣中铁元素质量分数为 (用最简分数表达式表示)。
32. (16分)(1) Al2O3 Fe2O3 + 6H+ ==2Fe3+ + 3H2O
(2)3.2—3.8 (3) SiO2 Al2(SO4)3 (4) 14m/15w
【解析】
试题分析:(1)硫酸渣中含Fe2O3、SiO2、Al2O3、MgO,属于两性氧化物的是Al2O3,氧化铁是碱性氧化物,可以和硫酸反应生成硫酸铁和水,即Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,离子反应方程式为:Fe2O3 + 6H+ ==2Fe3+ + 3H2O(2)根据几种离子沉淀的pH,使Fe3+沉淀完全的PH为3.2,其他离子开始沉淀PH为3.8,因此所选PH需介于3.2和3.8之间;答案为:3.2~3.8,(3)因二氧化硅不与硫酸反应,“滤渣A”主要成份的化学式为SiO2.未沉淀的离子为Na+、Mg2+、Al3+,滤液B可以回收的物质有Na2SO4、Al2(SO4)3、MgSO4;(4)铁红制备过程中,铁元素损耗25%,,最终得到铁红的质量为m kg,铁元素的质量为(1000m×112/160)÷75%=14m/15,则原来硫酸渣中铁元素质量分数为14m/15w。
考点:考查物质的性质,离子方程式的书写,元素及其化合物的性质等知识。

 阅读快车系列答案
阅读快车系列答案