题目内容
7.还原2.4molXO(OH)3+到X元素的低价态时,需消耗3mol/L的Na2SO3溶液2L,则在此反应中X元素的低价态为( )| A. | 0价 | B. | +1价 | C. | -1价 | D. | -2价 |
分析 Na2SO3还原2.4molXO(OH)3+到X元素的低价态,则Na2SO3被氧化为Na2SO4,反应中S元素的化合价由+4价升高为+6价,令X元素在还原产物中的化合价为a,根据电子转移守恒计算a的值.
解答 解:Na2SO3还原2.4molXO(OH)3+到X元素的低价态,则Na2SO3被氧化为Na2SO4,反应中S元素的化合价由+4价升高为+6价,
令X元素在还原产物中的化合价为a,
由电子守恒可知,2.4mol×(6-a)=2L×3mol•L-1×(6-4),
解得a=+1,
故选B.
点评 本题考查氧化还原反应的有关计算,为高频考点,把握反应中元素的化合价变化及电子守恒为解答的关键,题目难度不大,注意计算中守恒思想的运用.

练习册系列答案
相关题目
17.在通常条件下,下列各组中物质的性质排列正确的是( )
| A. | 热稳定性:HF>H2O>NH3 | B. | 溶解度:HCl>H2S>SO2 | ||
| C. | 半径:Al>Mg>Na | D. | 熔点:CO2>KCl>SiO2 |
2.下列物质与HNO3反应时,硝酸既表现出强氧化性又表现出酸性的是( )
| A. | Fe2O3 | B. | FeS | C. | Cu(OH)2 | D. | C |
12.分子式为C5H10的烯烃,考虑顺反异构的情况下,其同分异构体的数目为( )
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
19.A、B、C、D 四种原子序数小于18 的元素,其离子 aA+、bB2+、cC-、dD2-具有相同的电子层结构,下列判断正确的是( )
| A. | 原子序数的大小顺序是:B<A<C<D | |
| B. | 离子半径由大到小的顺序是:B2+>A+>C->D2- | |
| C. | A、B、C、D四种元素原子具有相同的电子层数 | |
| D. | 金属性A>B,非金属性C>D |
1.某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了下列实验.
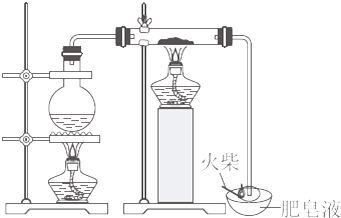
(1)用如图K8-2所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水反应).反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当肥皂泡破裂,有爆鸣声或“噗”的声音(填实验现象)时,
说明“铁与水蒸气”能够进行反应.
(2)为了证明反应后的固体混合物中含有+3价的Fe,他们计划取出少量混合物于试管中,加入足量的盐酸,溶解、过滤.向滤液中滴加KSCN溶液,观察溶液的颜色.在下表中填写滴加KSCN溶液后可能观察到的现象、结论与解释(可以不填满).
(3)将反应后固体溶于足量的盐酸中充分溶解,可选用c试剂证明溶液中含有Fe2+.
a.Cl2和KSCN溶液
b.NaOH溶液
c.KMnO4溶液.

(1)用如图K8-2所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水反应).反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当肥皂泡破裂,有爆鸣声或“噗”的声音(填实验现象)时,
说明“铁与水蒸气”能够进行反应.
(2)为了证明反应后的固体混合物中含有+3价的Fe,他们计划取出少量混合物于试管中,加入足量的盐酸,溶解、过滤.向滤液中滴加KSCN溶液,观察溶液的颜色.在下表中填写滴加KSCN溶液后可能观察到的现象、结论与解释(可以不填满).
| 现象 | 结论与解释 | |
| 可能① | 溶液变为红色 | 混合物中含有+3价Fe,因为Fe3+遇KSCN变红色 |
| 可能② | 溶液为浅绿色 | 反应后的固体中可能含有+3价Fe,也可能不含有+3价Fe,因为若铁剩余较多,可将溶液中的Fe3+还原为Fe2+ |
a.Cl2和KSCN溶液
b.NaOH溶液
c.KMnO4溶液.
 ②HCl
②HCl ③Cl2
③Cl2 ④CO2
④CO2 ⑤KCl
⑤KCl
 ②Br2
②Br2 .
.