题目内容
2.下列物质与HNO3反应时,硝酸既表现出强氧化性又表现出酸性的是( )| A. | Fe2O3 | B. | FeS | C. | Cu(OH)2 | D. | C |
分析 硝酸表现氧化性,则反应后N元素的化合价降低;表现出酸性,反应物中有硝酸盐生成.
解答 解:A.稀硝酸与Fe2O3反应反应生成硝酸铁和水,化合价没有变化,不是氧化还原反应,硝酸只表现出酸性,故A错误;
B.稀硝酸有氧化性,可同FeS发生氧化还原反应,生成S、硝酸铁、NO和水,硝酸既表现出强氧化性又表现出酸性,故B正确;
C.浓硝酸与氢氧化铜反应生成硝酸铜和水,N元素化合价不变,硝酸只表现出酸性,故C错误;
D.浓硝酸与灼热的碳反应生成二氧化碳、二氧化氮和水,硝酸只表现出强氧化性,故D错误;
故选B.
点评 本题考查硝酸的化学性质,把握硝酸的强氧化性、酸性、不稳定性为解答的关键,注意发生的氧化还原反应,选项C为易错点,题目难度不大.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
12.某多肽分子式为C46H71O24N13,完全水解后生成的产物为甘氨酸、丙氨酸、谷氨酸,则1mol该多肽彻底水解生成的谷氨酸(C5H9NO4)的物质的量为( )
| A. | 3mol | B. | 4mol | C. | 5mol | D. | 6mol |
13.不洁净玻璃仪器洗涤方法正确的是( )
| A. | 做银镜反应后的试管用氨水洗涤 | |
| B. | 做碘升华实验后的烧杯用酒精洗涤 | |
| C. | 盛装苯酚后的试管用盐酸洗涤 | |
| D. | 收集完乙酸乙酯的试管用碳酸钠溶液洗涤 |
17.下表是元素周期表的一部分,请回答有关问题:
(1)这10种元素分别为:①O②F③Na④Mg⑤P⑥S⑦Cl⑧Ar⑨K⑩Br(用元素符号表示);
(2)③、④、⑨三种元素按原子半径由大到小的顺序排列为K>Na>Mg,这三种元素的最高价氧化物的水化物中,按碱性由强到弱顺序排列为KOH>NaOH>Mg(OH)2(用化学式表示);
(3)①对应元素名称为氧,在元素周期表中所处位置为第二周期ⅥA族其氢化物与③反应的化学方程式为2Na+2H2O=2NaOH+H2↑;
(4)⑤、⑥、⑦三种元素的最高价氧化物的水化物酸性由强到弱顺序排列为HClO4>H2SO4>H3PO4;②、⑦、⑩氢化物稳定性由强到弱顺序排列为HF>HCl>HBr(用化学式表示);
(5)③元素与⑦元素两者核电荷数之差是6.
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)③、④、⑨三种元素按原子半径由大到小的顺序排列为K>Na>Mg,这三种元素的最高价氧化物的水化物中,按碱性由强到弱顺序排列为KOH>NaOH>Mg(OH)2(用化学式表示);
(3)①对应元素名称为氧,在元素周期表中所处位置为第二周期ⅥA族其氢化物与③反应的化学方程式为2Na+2H2O=2NaOH+H2↑;
(4)⑤、⑥、⑦三种元素的最高价氧化物的水化物酸性由强到弱顺序排列为HClO4>H2SO4>H3PO4;②、⑦、⑩氢化物稳定性由强到弱顺序排列为HF>HCl>HBr(用化学式表示);
(5)③元素与⑦元素两者核电荷数之差是6.
7.还原2.4molXO(OH)3+到X元素的低价态时,需消耗3mol/L的Na2SO3溶液2L,则在此反应中X元素的低价态为( )
| A. | 0价 | B. | +1价 | C. | -1价 | D. | -2价 |
11.有关晶体结构的叙述中,错误的是( )
| A. | 金刚石的网状结构中,最小的环上有6个碳原子 | |
| B. | 分子晶体熔化时,不破坏共价键;原子晶体熔化时,破坏共价键 | |
| C. | 在金属铜的晶体中,由于存在自由电子,因此铜能导电 | |
| D. | 在氯化铯晶体中,每个氯离子周围最近且等距离的氯离子有8个 |
12.下表是第三周期部分主族元素的电离能数据:
下列说法不正确的是( )
| 元素 | I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 甲 | 495.8 | 4562 | 6910.3 | 9543 | 13354 |
| 乙 | 577.5 | 1816.7 | 2744.8 | 11577 | 14842 |
| 丙 | 786.5 | 1577.1 | 3231.6 | 4355.5 | 16091 |
| 丁 | 1251.2 | 2298 | 3822 | 5158.6 | 6542 |
| A. | 甲的金属性比乙强,且甲和乙的最高价氧化物的水化物可以相互反应 | |
| B. | 乙的最外层电子轨道表达式: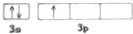 | |
| C. | 丙的最高价氧化物性质稳定,属于原子晶体,常温下不和强酸、强碱、强氧化剂反应 | |
| D. | 丁的常见的气态氢化物一定是极性分子 |
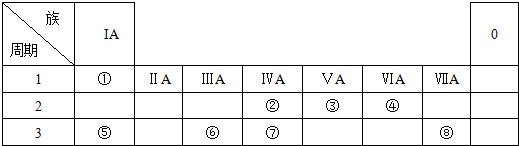
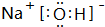
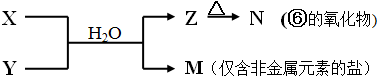
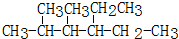
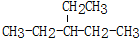 .
.