题目内容
6.下列反应中调节反应物用量或浓度不会改变反应产物的是( )| A. | 铜粉加入硝酸中 | B. | 溴化亚铁溶液中通氯气 | ||
| C. | AlCl3溶液中滴入NaOH 溶液 | D. | 铁粉在硫蒸气中燃烧 |
分析 A.铜与浓硝酸应生成NO2与稀硝酸反应NO;
B.亚铁离子、溴离子均能被氯气氧化,还原性强的先被氧化,向溴化亚铁溶液中通入氯气,氯气先和亚铁离子反应,当亚铁离子完全反应后,氯气再和溴离子反应;
C.向一定量的氯化铝溶液中滴加一定浓度的氢氧化钠溶液,首先发生反应Al3++3OH-=Al(OH)3↓,Al3+反应完毕,继续滴加NaOH溶液,发生反应OH-+Al(OH)3=AlO2-+H2O;
D.铁与硫反应生成硫化亚铁.
解答 解:A.铜和硝酸溶液反应,如果是浓硝酸,生成NO2,如果是稀硝酸,生成NO,故A不选;
B.向溴化亚铁溶液中通入氯气,氯气先和亚铁离子反应,2Fe2++Cl2═2Fe3++2Cl-,当亚铁离子完全反应后,氯气再和溴离子反应,Cl2+2Br-═2Cl-+Br2,所以氯气量的多少决定产物的成分,故B不选;
C.向一定量的氯化铝溶液中滴加一定浓度的氢氧化钠溶液,首先发生反应Al3++3OH-=Al(OH)3↓,Al3+反应完毕,继续滴加NaOH溶液,发生反应OH-+Al(OH)3=AlO2-+H2O,过量氢氧化钠反应先生成沉淀,后沉淀溶解,少量氢氧化钠只生成沉淀,故C不选;
D.硫的氧化性弱与变价金属反应生成低价硫化物,铁与硫反应生成硫化亚铁,与反应物的用量或浓度无关,故D选;
故选:D.
点评 本题考查了物质的用量或浓度不同导致产物不同,明确物质之间的反应是解本题的关键,易错选项是D,注意硫的氧化性弱与变价金属反应生成低价硫化物,题目难度不大.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
16.下列有关仪器的名称、图形、操作的叙述均正确的是( )
| 选项 | A | B | C | D |
| 名称 | 250mL容量瓶 | 分液漏斗 | 酸式滴定管 | 冷凝管 |
| 图形 |  |  |  | 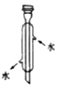 |
| 操作 | 定容时仰视刻度, 则配得的溶液浓 度偏小 | 用酒精萃取水中 碘从上倒出 | 可用于量取 Na2CO3溶液 | 蒸馏实验中将 蒸气冷凝为液体 |
| A. | A | B. | B | C. | C | D. | D |
14.下列有关性质的比较,错误的是( )
| A. | 酸性:H2SO4>H2CO3 | B. | 沸点:CBr4>CCl4 | ||
| C. | 碱性:Al(OH)3>NaOH | D. | 热稳定性:HF>HCl |
11.不能通过化合反应得到的是( )
| A. | NH4Cl | B. | Cu2S | C. | FeCl2 | D. | Al(OH)3 |
18.2016年11月,我国首枚大型运载火箭“长征5号”成功发射.该火箭主发动机中所用的液氧(O2)属于( )
| A. | 单质 | B. | 氧化物 | C. | 化合物 | D. | 有机物 |
8.不能说明金属性Na>Mg>Al的是( )
| A. | 原子半径Na>Mg>Al | |
| B. | 碱性NaOH>Mg(OH)2>Al (OH)3 | |
| C. | 阳离子的氧化性Na+<Mg2+<Al3+ | |
| D. | Na与冷水剧烈反应,Mg与冷水反应微弱;镁粉与铝粉分别与同浓度稀HCl反应,镁粉比铝粉反应剧烈 |