题目内容
2.硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业.SnSO4的实验室制备设计路线如下:下列有关说法正确的是( )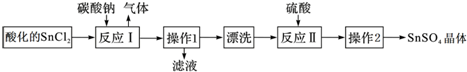
| A. | SnCl2酸化是为了防止溶解时发生水解 | |
| B. | 反应I中发生的离子反应为:CO32-+2H+=CO2↑+H2O | |
| C. | 漂洗时,将固体置于烧杯中,加蒸馏水洗涤过滤2~3次 | |
| D. | 操作1为过滤,操作2为结晶 |
分析 SnCl2溶解得到溶液加入碳酸钠沉淀锡离子,过滤得到沉淀洗涤后加入硫酸溶解得到硫酸锡溶液,蒸发浓缩冷却结晶,过滤洗涤得到硫酸锡晶体;
A.SnCl2易水解,加入盐酸,抑制Sn2+水解;
B.反应Ⅰ得到沉淀是SnO,Sn元素化合价不变化,同时生成气体,该气体为二氧化碳;
C.洗涤在分液漏斗中进行;
D.由以上分析可知操作1为过滤,操作2为结晶;
解答 解:A.SnCl2易水解,酸化是为了防止溶解时发生水解,故A正确;
B.反应Ⅰ得到沉淀是SnO,Sn元素化合价不变化,同时生成气体,该气体为二氧化碳,离子方程式为:Sn2++CO32-═SnO↓+CO2↑,顾B错误;
C.洗涤在分液漏斗中进行,加蒸馏水洗涤过滤2~3次,故C错误;
D.操作1为过滤,操作2为结晶,故D正确;
故选AD.
点评 本题以SnSO4制备为载体,考查学生对工艺流程的理解、物质的分离提纯、阅读题目获取信息的能力、难度中等,对学生的基础知识及逻辑推理有较高的要求.

练习册系列答案
相关题目
19.下列说法错误的是( )
| A. | NaHCO3溶液加水稀释,$\frac{c(N{a}^{+})}{c(HC{{O}_{3}}^{-})}$的比值保持增大 | |
| B. | 在0.1 mol•L一1氨水中滴加0.lmol•L一1盐酸,恰好完全中和时溶液的pH<7 | |
| C. | 向0.lmol/L Na2S03溶液中加人少量NaOH固体,c(Na+)、c(SO32-)均增大 | |
| D. | 0.lmol•L一1氨水加水稀释,溶液中c(H+)和c(OH-)都减小 |
20.维通橡胶是一种耐腐蚀、耐油、耐高温、耐寒性能都特别好的氟橡胶.它的结构简式为 ,则合成它的单体是( )
,则合成它的单体是( )
 ,则合成它的单体是( )
,则合成它的单体是( )| A. | 氟乙烯和全氟丙烯 | B. | 1,1-二氟乙烯和全氟丙烯 | ||
| C. | 全氟异戊二烯 | D. | 1-三氟甲基-1,3-丁二烯 |
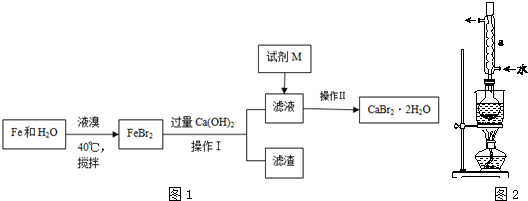
10.正溴丁烷(CH3CH2CH2CH2Br)是一种重要的有机合成工业原料.在实验中可利用如图1装置(加热或夹持装置省略)制备正溴丁烷.制备时的化学反应方程式及有关数据如下:NaBr+H2SO4=HBr+NaHSO4
C4H9OH+HB$\stackrel{浓硫酸}{→}$rC4H9Br+H2O
实验步骤:在装置A中加入2mL水,并小心加入28mL浓硫酸,混合均匀后冷却至室温.再依次加入18.5mL正丁醇和26g溴化钠,充分摇振后加入沸石,连接气体吸收装置C.将装置A置于石棉网上加热至沸腾,然后调节为小火使反应物保持平稳地回流.一段时间后停止加热,待反应液冷却后,拆去装置B,改为蒸馏装置,蒸出粗正溴丁烷.
请回答下列问题;
(1)仪器A的名称是圆底烧瓶,仪器B的作用是冷却、回流.操作中加入沸石的作用是防止暴沸.
(2)装置C中盛装的液体是NaOH溶液,其作用是吸收逸出的溴化氢,防止其污染空气.
(3)制备的粗产物正溴丁烷中往往含有水分、正丁醇等杂质,加入干燥剂出去水分后,再由图2操作中的d制备纯净的正溴丁烷.
(4)若制备实验的“回流”过程中不采用“调节为小火”,仍采用大火加热回流,则会使产品产率偏低(填“高”或“低”),试说出其中一种原因:大火,副反应多或产物逸出较多.
(5)若最终得到13.6g纯净的正溴丁烷,则该实验的产率是49.6%(保留三位有效数字)

C4H9OH+HB$\stackrel{浓硫酸}{→}$rC4H9Br+H2O
| 物质 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 水中溶解性 |
| 正丁醇 | 74 | 0.80 | 117.3 | 微溶 |
| 正溴丁烷 | 137 | 1.27 | 101.6 | 难溶 |
| 溴化氢 | 81 | --- | --- | 极易溶解 |
请回答下列问题;
(1)仪器A的名称是圆底烧瓶,仪器B的作用是冷却、回流.操作中加入沸石的作用是防止暴沸.
(2)装置C中盛装的液体是NaOH溶液,其作用是吸收逸出的溴化氢,防止其污染空气.
(3)制备的粗产物正溴丁烷中往往含有水分、正丁醇等杂质,加入干燥剂出去水分后,再由图2操作中的d制备纯净的正溴丁烷.
(4)若制备实验的“回流”过程中不采用“调节为小火”,仍采用大火加热回流,则会使产品产率偏低(填“高”或“低”),试说出其中一种原因:大火,副反应多或产物逸出较多.
(5)若最终得到13.6g纯净的正溴丁烷,则该实验的产率是49.6%(保留三位有效数字)

17.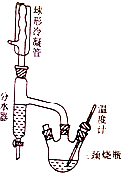 实验室制备正丁醚的原理如下:
实验室制备正丁醚的原理如下:
2CH3CH2CH2OH$\stackrel{H_{2}SO_{4},134-135℃}{?}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
温度高于135℃会发生副反应生成丁烯.相关物质的物理性质如下表:
实验步骤如下(装置如图所示):
a.在100mL三颈烧瓶中加入36.5mL正丁醇和约10mL浓硫酸,混合均匀,并加入几粒沸石.
b.在三颈烧瓶的一瓶口装上温度计,另一瓶口装上分水器,分水器上端接回流冷凝管.
c.在分水管中放置2mL水,然后加热到134-135℃,回流,可观察到分水器中水面缓慢上升.
d.实验结束后,冷却反应物,然后将反应后的混合液体倒入35mL水中,充分振摇,静置后分液,分出粗产品.
试回答:
(1)温度高于135℃时所发生反应的化学方程式为CH3CH2CH2CH2OH$→_{高于135℃}^{浓H_{2}SO_{4}}$CH3CH2CH=CH2↑+H2O;
(2)实验中为控制温度在134-135℃,最好选用的加热方式为③;
①水浴 ②砂浴 ③油浴
(3)为提纯粗产品,分别进行了①加入无水氯化钙、②水洗、③碳酸氢钠溶液洗涤,则正确的操作顺序为③②①,其中使用碳酸氢钠溶液洗涤的目的是去除反应的催化剂硫酸,进行水洗时,所用的主要玻璃仪器名称为分液漏斗,该仪器在使用前需要时行的操作是检漏.
(4)在该实验过程中,判断反应基本进行完全的现象是分水器中液面不再上升;
(5)若最终得到13.0g正丁醚,则该实验的产率为50.0%.
 实验室制备正丁醚的原理如下:
实验室制备正丁醚的原理如下:2CH3CH2CH2OH$\stackrel{H_{2}SO_{4},134-135℃}{?}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
温度高于135℃会发生副反应生成丁烯.相关物质的物理性质如下表:
| 物质 | 密度/g•mL-1 | 熔点/℃ | 沸点/℃ | 水溶性 |
| 正丁醇 | 0.81 | -89.8 | 117.7 | 微溶于水 |
| 正丁醚 | 0.769 | -98 | 142 | 不溶于水 |
a.在100mL三颈烧瓶中加入36.5mL正丁醇和约10mL浓硫酸,混合均匀,并加入几粒沸石.
b.在三颈烧瓶的一瓶口装上温度计,另一瓶口装上分水器,分水器上端接回流冷凝管.
c.在分水管中放置2mL水,然后加热到134-135℃,回流,可观察到分水器中水面缓慢上升.
d.实验结束后,冷却反应物,然后将反应后的混合液体倒入35mL水中,充分振摇,静置后分液,分出粗产品.
试回答:
(1)温度高于135℃时所发生反应的化学方程式为CH3CH2CH2CH2OH$→_{高于135℃}^{浓H_{2}SO_{4}}$CH3CH2CH=CH2↑+H2O;
(2)实验中为控制温度在134-135℃,最好选用的加热方式为③;
①水浴 ②砂浴 ③油浴
(3)为提纯粗产品,分别进行了①加入无水氯化钙、②水洗、③碳酸氢钠溶液洗涤,则正确的操作顺序为③②①,其中使用碳酸氢钠溶液洗涤的目的是去除反应的催化剂硫酸,进行水洗时,所用的主要玻璃仪器名称为分液漏斗,该仪器在使用前需要时行的操作是检漏.
(4)在该实验过程中,判断反应基本进行完全的现象是分水器中液面不再上升;
(5)若最终得到13.0g正丁醚,则该实验的产率为50.0%.
14.在浓盐酸中H3AsO3与SnCl2反应的离子方程式为3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M.下列关于该反应的说法中,错误的是( )
| A. | M为H2O | |
| B. | 每还原1 mol氧化剂,就有3 mol电子转移 | |
| C. | 还原性:SnCl2>As | |
| D. | 氧化产物和还原产物的物质的量之比为2:3 |
11.76.8mg铜与适量浓硝酸反应,铜全部作用后,如果NO3-离子减少2×10-3mol,则溶液中H+离子同时减少( )
| A. | 4.8×10-3mol | B. | 4.4×10-3mol | C. | 3.2×10-3mol | D. | 2.2×10-3mol |
12.与50mL 0.1mol•L-1Na2CO3溶液中 Na+ 的物质的量浓度相同的溶液是( )
| A. | 50mL 0.2mol•L-1 的 NaCl 溶液 | |
| B. | 100mL 0.1mol•L-1 的 NaCl 溶液 | |
| C. | 25mL 0.2mol•L-1 的 Na2SO4 溶液 | |
| D. | 10mL 0.5mol•L-1 的 Na2CO3 溶液 |