题目内容
12.与50mL 0.1mol•L-1Na2CO3溶液中 Na+ 的物质的量浓度相同的溶液是( )| A. | 50mL 0.2mol•L-1 的 NaCl 溶液 | |
| B. | 100mL 0.1mol•L-1 的 NaCl 溶液 | |
| C. | 25mL 0.2mol•L-1 的 Na2SO4 溶液 | |
| D. | 10mL 0.5mol•L-1 的 Na2CO3 溶液 |
分析 根据电解质溶液离子浓度=电解质浓度×电解质电离产生的该离子的数目.
解答 解:50mL 0.1mol•L-1 Na2CO3溶液中Na+的物质的量浓度为0.2mol/L,
A.50 mL 0.2 mol•L-1的NaCl溶液中Na+的物质的量浓度为0.2mol/L,故A正确;
B.100 mL 0.1 mol•L-1的NaCl溶液中Na+的物质的量浓度为0.1mol/L,故B错误;
C.25 mL 0.2 mol•L-1的Na2SO4溶液中Na+的物质的量浓度为0.4mol/L,故C错误;
D.10 mL 0.5 mol•L-1的Na2CO3溶液中Na+的物质的量浓度为1mol/L,故D错误.
故选A.
点评 本题考查物质的量浓度的计算与理解,题目难度不大,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.

练习册系列答案
相关题目
2.硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业.SnSO4的实验室制备设计路线如下:下列有关说法正确的是( )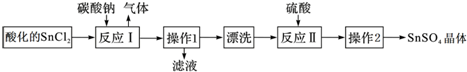

| A. | SnCl2酸化是为了防止溶解时发生水解 | |
| B. | 反应I中发生的离子反应为:CO32-+2H+=CO2↑+H2O | |
| C. | 漂洗时,将固体置于烧杯中,加蒸馏水洗涤过滤2~3次 | |
| D. | 操作1为过滤,操作2为结晶 |
20.下列物质中,不可以通过乙烯加成反应得到的是( )
| A. | CH3CH3 | B. | CH3CHCl2 | C. | CH3CH2OH | D. | CH3CH2Br |
7.下列各组物质中,最简式相同,但既不是同系物,又不是同分异构体的是( )
| A. | 甲醛﹑甲酸甲酯 | B. | 丙烯﹑环丙烷 | C. | 乙酸﹑甲酸甲酯 | D. | 乙烯﹑1-丁烯 |
17.下列物质间的转化,不可能通过一步反应实现的是( )
| A. | Cu---Cu(OH)2 | B. | H2O2--O2 | C. | CaCO3---CaCl2 | D. | K2CO3--KCl |
4.下列热化学方程式或说法正确的是( )
| A. | 甲烷的燃烧热为△H=-890kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890 kJ?mol-1 | |
| B. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: N2(g)+3H2(g)$?_{500℃,30MPa}^{催化剂}$2NH3(g)△H=-38.6kJ?mol-1 | |
| C. | 已知:H2(g)+F2(g)═2HF(g);△H=-270 kJ/mol,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | |
| D. | 在C中相同条件下,2 mol HF气体的能量小于1 mol氢气与1 mol氟气的能量总和 |
1.某物质灼烧时,焰色反应为黄色,下列判断正确的是( )
| A. | 该物质一定是钠的化合物 | B. | 该物质一定是金属钠 | ||
| C. | 该物质一定含钠元素 | D. | 该物质可能含钾元素 |
2.在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的有( )
| A. | 滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl-、N03- | |
| B. | pH为11的溶液:S2-、SO32-、SO42-、Na+ | |
| C. | 水电离出来的c (H+)=10-13 mol/L的溶液:K+、HCO3一、Br一、Ba2+ | |
| D. | 无色溶液:K+、CO32-、N03-、Ca2+ |
 A、B、C、D、E、F六种物质的相互转化关系如附图所示(反应条件未标出).
A、B、C、D、E、F六种物质的相互转化关系如附图所示(反应条件未标出).