题目内容
11.76.8mg铜与适量浓硝酸反应,铜全部作用后,如果NO3-离子减少2×10-3mol,则溶液中H+离子同时减少( )| A. | 4.8×10-3mol | B. | 4.4×10-3mol | C. | 3.2×10-3mol | D. | 2.2×10-3mol |
分析 反应中硝酸起氧化剂与酸的作用,NO3-减少2×10-3mol,说明起氧化剂作用的硝酸为2×10-3mol,根据Cu元素守恒计算硝酸铜的物质的量,再根据硝酸根守恒计算起酸性作用的硝酸,溶液中减少的氢离子的物质的量等于参加反应硝酸的物质的量.
解答 解:反应中硝酸起氧化剂与酸的作用,NO3-减少2×10-3mol,说明起氧化剂作用的硝酸为2×10-3mol,76.8mgCu的物质的量=$\frac{76.8×10{\;}^{-3}g}{64g/mol}$=0.0012mol,则硝酸铜物质的量0.0012mol,由硝酸根守恒离子,其酸性作用的硝酸为0.0012mol×2=0.0024mol,故参加反应硝酸为2×10-3mol+0.0024mol=4.4×10-3mol,故溶液中溶液中H+减少了4.4×10-3mol,
故选B.
点评 本题考查化学方程式有关计算,难度中等,注意利用守恒思想解答,避免判断生成的气体而简化计算.

练习册系列答案
相关题目
8.如果某元素的化合价由化合态变为游离态,则它( )
| A. | 有可能被氧化,也有可能被还原 | B. | 被氧化 | ||
| C. | 由高价变为零价 | D. | 被还原 |
2.硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业.SnSO4的实验室制备设计路线如下:下列有关说法正确的是( )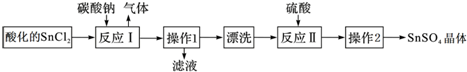

| A. | SnCl2酸化是为了防止溶解时发生水解 | |
| B. | 反应I中发生的离子反应为:CO32-+2H+=CO2↑+H2O | |
| C. | 漂洗时,将固体置于烧杯中,加蒸馏水洗涤过滤2~3次 | |
| D. | 操作1为过滤,操作2为结晶 |
19.描述分子结构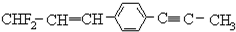 的下列叙述中,正确的是( )
的下列叙述中,正确的是( )
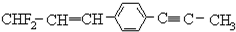 的下列叙述中,正确的是( )
的下列叙述中,正确的是( )| A. | 12个碳原子不可能都在同一平面上 | |
| B. | 处于同一直线上的原子最多有4个 | |
| C. | 处在同一平面上的原子最多有20个 | |
| D. | 除苯环外的其余碳原子有可能都在同一直线上 |
6.短周期元素A、B、C原子序数依次递增,它们原子的最外层电子数之和为10,A与C同主族,B原子最外层电子数等于A原子次外层电子数,则下列叙述正确的是( )
| A. | 原子半径A<B<C | |
| B. | A的氢化物的稳定性大于C的氢化物 | |
| C. | A的氧化物是离子化合物,B的氧化物是共价化合物 | |
| D. | A与C可形成离子化合物 |
16.在一定温度下的定容密闭容器中,下列情况能表明可逆反应:H2(g)+I2(g)?2HI(g)已达平衡的是( )
| A. | H2的生成速率与I2的生成速率相等 | |
| B. | 若单位时间内生成n mol H2的同时生成2n mol HI | |
| C. | H2、I2、HI的浓度相等 | |
| D. | 反应容器内的压强不随时间的变化而变化 |
20.下列物质中,不可以通过乙烯加成反应得到的是( )
| A. | CH3CH3 | B. | CH3CHCl2 | C. | CH3CH2OH | D. | CH3CH2Br |
1.某物质灼烧时,焰色反应为黄色,下列判断正确的是( )
| A. | 该物质一定是钠的化合物 | B. | 该物质一定是金属钠 | ||
| C. | 该物质一定含钠元素 | D. | 该物质可能含钾元素 |
 A、B、C、D、E、F六种物质的相互转化关系如附图所示(反应条件未标出).
A、B、C、D、E、F六种物质的相互转化关系如附图所示(反应条件未标出).