题目内容
3.工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g)?2NH3(g).Ⅰ、其部分工艺流程如右图所示,反应体系中各组分的部分性质见下表:

| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210 | -253 | -78 |
| 沸点(℃) | -195 | -259 | -33 |
(1)写出该反应的化学平衡常数表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$.随着温度的升高,K值减小(填增大、减小、不变).平衡常数K值越大,表明AB(填序号).
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(2)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程.即反应后通过把混合气体的温度降低到-33.42使NH3分离出来;继续循环的气体是N2、H2.
Ⅱ、在一密闭容器中发生该反应,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
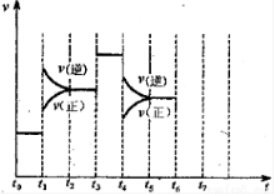
(3)t1、t3、t4时刻分别改变的一个条件是:t1时刻C;t3时刻E;t4时刻B(填选项).
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(4)依据(2)中的结论,下列时间段中,氨的百分含量最高的是A(填选项).
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6.
分析 (1)依据化学方程式和平衡常数概念书写,平衡常数等生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积,反应是放热反应,随温度升高,平衡逆向进行;平衡常数是衡量反应进行程度的物理量,平衡常数K值越大,说明正向进行程度越大;
(2)减少生成物的浓度,化学平衡向着正向移动,氨气易液化;
(3)由图可知,t1正逆反应速率均增大,且逆反应速率大于正反应速率;t3正逆反应速率同等程度的增大;t4时正逆反应速率均减小,且逆反应速率大于正反应速率;
(4))由图可知,t1平衡逆向移动,t3不移动,t4平衡逆向移动,根据移动结果分析.
解答 解:①,工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g)?2NH3(g),△H=-92.44kJ/mol,平衡常数为K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$,反应是放热反应,随着温度的升高平衡逆向进行,平衡常数减小;平衡常数K值越大反应这些进行的程度越大,
A.正向进行越大,N2的转化率越高,故A正确;
B.反应正向进行,生成的氨气越多,NH3的产率越大,故B正确;
C.反应正向进行,原料中N2的含量减少,故C错误;
D.平衡常数越大,说明正向进行程度越大,但化学反应速率不一定越快,故D错误;
故答案为:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$;减小;A B;
(2)根据题意可知氨气的沸点是-33.42,可以将温度降低到-33.42,让氨气分离出来,氢气和氮气可以再循环利用,故答案为:-33.42;NH3;N2、H2;
(3)由N2(g)+3H2(g)?2NH3(g)△H<0,可知,该反应为放热反应,且为气体体积减小的反应,则由图可知,t1正逆反应速率均增大,且逆反应速率大于正反应速率,改变条件应为升高温度;
t3正逆反应速率同等程度的增大,改变条件应为使用催化剂;
t4时正逆反应速率均减小,且逆反应速率大于正反应速率,改变条件应为减小压强,
故答案为:C;E;B;
(4)由图可知,t1平衡逆向移动,t3不移动,t4平衡逆向移动,均使氨气的含量减少,则t0~t1氨气的含量最大,故答案为:A.
点评 本题是一道关于化学平衡的题目,可以根据所学知识进行回答,难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 相同 | B. | 磁铁矿石高 | C. | 赤铁矿石高 | D. | 无法比较 |
①氯化铝溶液中滴加氢氧化钠溶液,②偏铝酸钠溶液中加盐酸,③氢氧化钠溶液中滴加氯化铝溶液,④氯化铝溶液中滴加氨水.
| A. | ①② | B. | ②③④ | C. | ①②④ | D. | ③④ |
 质量分数为a%的氨水,物质的量浓度为c1 mol•L-1,质量分数为2a%的氨水,物质的量浓度为c2 mol•L-1,则c1和c2的数值关系是( )
质量分数为a%的氨水,物质的量浓度为c1 mol•L-1,质量分数为2a%的氨水,物质的量浓度为c2 mol•L-1,则c1和c2的数值关系是( )| A. | c2=2c1 | B. | c2>2c1 | C. | c2<2c1 | D. | 无法确定 |
| A. | 小于0.8 g•cm-3 | B. | 大于1.0 g•cm-3 | ||
| C. | 介于0.8~1.0 g•cm-3 | D. | 无法推测 |

