题目内容
7.如图所示是分离混合物时常用的仪器,回答下列问题:
①写出仪器A、C、E的名称蒸馏烧瓶、分液漏斗、冷凝管.
②分离以下混合物应该主要选用上述什么仪器?(填字母符号)A.粗盐和泥沙:BDB.花生油和水:C.
分析 ①根据仪器的图形判断仪器的种类;
②泥沙不溶于水,可用过滤的方法分离,花生油不溶于水,可用分液的方法分离.
解答 解:①A仪器是蒸馏烧瓶,用于蒸馏实验;B仪器是漏斗,用于过滤实验;C仪 器是分液漏斗,用于萃取分液实验;D仪器是蒸发皿,用于蒸发实验;E仪器是冷凝管,用于蒸馏实验,故答案为:蒸馏烧瓶;分液漏斗;冷凝管;
②粗盐和泥沙必须通过溶解过滤除去泥沙,再蒸发结晶得到食盐,要用到漏斗和蒸发皿,故选BD;花生油和水不互溶的两种液体,用分液的方法分离,可选用分液漏斗,故选C.
故答案为:BD;C.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析、实验能力的考查,注意把握物质的性质以及操作的原理、方法,难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
18.2008年10月8日,美籍华裔科学家钱永健获得2008年度诺贝尔化学奖.16岁时,他凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获“美国西屋科学天才奖”.下列叙述正确的是( )
| A. | 金属腐蚀就是金属失去电子被还原的过程 | |
| B. | 合金的熔点都高于它的成分金属,合金的耐腐蚀性也都比其成分金属强 | |
| C. | 铜板上的铁铆钉处在潮湿的空气中直接发生反应:Fe-3e-=Fe3+,继而形成铁锈 | |
| D. | 将水库中的水闸(钢板)与外加直流电源的负极相连,正极连接到一块废铁上可防止水闸被腐蚀 |
2.工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图1:
(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),反应的平衡常数随温度的变化如表:
从表可以推断:此反应是放(填“吸”或“放”)热反应.400℃时,H2浓度为2mol/L,CO2浓度为1.5mol/L,H2O浓度为3mol/L,CO浓度为1mol/L,则下一时刻,反应向正向(填”正向”或”逆向”)进行.
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第Ⅱ步反应,达到平衡后下列关系正确的是AD.
A.2c1=c2=c3 B.2Q1=Q2=Q3 C.α1=α2=α3 D.α1+α2=1
(3)在一个绝热等容容器中,不能判断此流程的第Ⅱ步反应达到平衡的是②③.
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化 ⑥v(CO2)正=v(H2O)逆
(4)如图2表示此流程的第Ⅱ步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是降低温度、增加水蒸汽的量(或减少氢气的量)(写出两种).若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变).
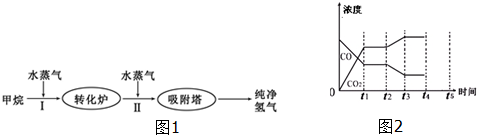
(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),反应的平衡常数随温度的变化如表:
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第Ⅱ步反应,达到平衡后下列关系正确的是AD.
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| A | 1、1、0、0 | c1 | Q1 | α1 |
| B | 0、0、2、2 | c2 | Q2 | α2 |
| C | 2、2、0、0 | c3 | Q3 | α3 |
(3)在一个绝热等容容器中,不能判断此流程的第Ⅱ步反应达到平衡的是②③.
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化 ⑥v(CO2)正=v(H2O)逆
(4)如图2表示此流程的第Ⅱ步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是降低温度、增加水蒸汽的量(或减少氢气的量)(写出两种).若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变).

3.工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g)?2NH3(g).
Ⅰ、其部分工艺流程如右图所示,反应体系中各组分的部分性质见下表:

回答下列问题:
(1)写出该反应的化学平衡常数表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$.随着温度的升高,K值减小(填增大、减小、不变).平衡常数K值越大,表明AB(填序号).
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(2)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程.即反应后通过把混合气体的温度降低到-33.42使NH3分离出来;继续循环的气体是N2、H2.
Ⅱ、在一密闭容器中发生该反应,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
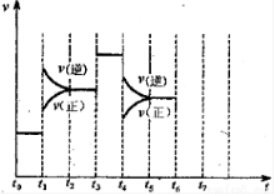
(3)t1、t3、t4时刻分别改变的一个条件是:t1时刻C;t3时刻E;t4时刻B(填选项).
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(4)依据(2)中的结论,下列时间段中,氨的百分含量最高的是A(填选项).
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6.
Ⅰ、其部分工艺流程如右图所示,反应体系中各组分的部分性质见下表:

| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210 | -253 | -78 |
| 沸点(℃) | -195 | -259 | -33 |
(1)写出该反应的化学平衡常数表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$.随着温度的升高,K值减小(填增大、减小、不变).平衡常数K值越大,表明AB(填序号).
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(2)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程.即反应后通过把混合气体的温度降低到-33.42使NH3分离出来;继续循环的气体是N2、H2.
Ⅱ、在一密闭容器中发生该反应,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:

(3)t1、t3、t4时刻分别改变的一个条件是:t1时刻C;t3时刻E;t4时刻B(填选项).
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(4)依据(2)中的结论,下列时间段中,氨的百分含量最高的是A(填选项).
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6.
5.一种全天候太阳能电化学电池的工作原理如图所示.下列说法错误的是( )


| A. | 该电池与硅太阳能电池供电原理相同 | |
| B. | 光照时,b极周围pH减小 | |
| C. | 光照时,H+由b极室透过质子膜进入a极室 | |
| D. | 夜间无光照时,a为电池的负极 |
 ;元素C的原子组成符号是2713Al.
;元素C的原子组成符号是2713Al.

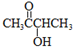 .
. CH3COO-+NH4++2Ag↓+3NH3+H2O.
CH3COO-+NH4++2Ag↓+3NH3+H2O. .
. .
. .
.