题目内容
4.含Fe3O470%的磁铁矿石和含Fe2O380%的赤铁矿石中的含铁百分率( )| A. | 相同 | B. | 磁铁矿石高 | C. | 赤铁矿石高 | D. | 无法比较 |
分析 设矿石均为100g,含Fe3O470%的磁铁矿石中四氧化三铁为70g,含Fe2O380%的赤铁矿石中氧化铁的质量为80g,结合Fe元素的含量计算.
解答 解:设矿石均为100g,含Fe3O470%的磁铁矿石中四氧化三铁为70g,含Fe的质量为70g×$\frac{56×3}{56×3+16×4}$×100%=20.52g,
含Fe2O380%的赤铁矿石中氧化铁的质量为80g,含Fe的质量为80g×$\frac{56×2}{56×2+16×3}$×100%=56g,
显然矿石质量相同时,赤铁矿石中的含铁百分率高,
故选C.
点评 本题考查元素质量分数的计算,为高频考点,把握化学式及元素质量分数计算方法为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
14.用质量均为100g的铜片作电极,电解AgNO3溶液,电解一段时间后两极质量相差28g,此时阳极质量为( )
| A. | 121.6 g | B. | 93.6 g | C. | 89.6 g | D. | 88.2 g |
3.工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g)?2NH3(g).
Ⅰ、其部分工艺流程如右图所示,反应体系中各组分的部分性质见下表:

回答下列问题:
(1)写出该反应的化学平衡常数表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$.随着温度的升高,K值减小(填增大、减小、不变).平衡常数K值越大,表明AB(填序号).
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(2)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程.即反应后通过把混合气体的温度降低到-33.42使NH3分离出来;继续循环的气体是N2、H2.
Ⅱ、在一密闭容器中发生该反应,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
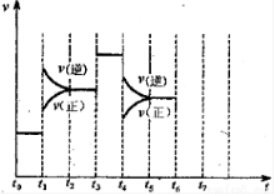
(3)t1、t3、t4时刻分别改变的一个条件是:t1时刻C;t3时刻E;t4时刻B(填选项).
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(4)依据(2)中的结论,下列时间段中,氨的百分含量最高的是A(填选项).
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6.
Ⅰ、其部分工艺流程如右图所示,反应体系中各组分的部分性质见下表:

| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210 | -253 | -78 |
| 沸点(℃) | -195 | -259 | -33 |
(1)写出该反应的化学平衡常数表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$.随着温度的升高,K值减小(填增大、减小、不变).平衡常数K值越大,表明AB(填序号).
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(2)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程.即反应后通过把混合气体的温度降低到-33.42使NH3分离出来;继续循环的气体是N2、H2.
Ⅱ、在一密闭容器中发生该反应,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:

(3)t1、t3、t4时刻分别改变的一个条件是:t1时刻C;t3时刻E;t4时刻B(填选项).
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(4)依据(2)中的结论,下列时间段中,氨的百分含量最高的是A(填选项).
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6.
20.${\;}_{53}^{131}$I是常规核裂变产物之一,可以通过测定大气或水中的含量变化来监测核电站是否发生放射性物质泄漏.下列有关有叙述中错误的是( )
| A. | ${\;}_{55}^{131}$I的化学性质与${\;}_{53}^{127}$I是相同 | |
| B. | ${\;}_{53}^{131}$I的原子序数为53 | |
| C. | ${\;}_{53}^{131}$I的原子核外电子数为78 | |
| D. | ${\;}_{53}^{131}$I的原子核内中子数多于质子数 |


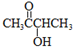 .
. CH3COO-+NH4++2Ag↓+3NH3+H2O.
CH3COO-+NH4++2Ag↓+3NH3+H2O. .
. .
. .
. 元素X、Y、Z、M、R均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4,且M原子的质子数是Y原子的2倍;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,请回答下列问题:
元素X、Y、Z、M、R均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4,且M原子的质子数是Y原子的2倍;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,请回答下列问题: .
. .
.