题目内容
某化学研究性学习小组拟对一种焰火原料(由两种短周期的常见金属单质组成的合金粉末)进行探究.请完成下列探究报告.
【探究目的】探究该焰火原料的组成
【资料检索】①Mg2+检验方法:取2滴待检液,加入2滴2mol?L-1 NaOH溶液,再加入1滴镁试剂(Ⅰ)染料(对硝基苯偶氮苯二酚).若出现沉淀并吸附镁试剂(Ⅰ)染料呈天蓝色,表示待检液中含有Mg2+.Ag+、Cu2+、Fe3+、NH4+会妨碍Mg2+检出.
②Mg(OH)2可溶于浓的氯化铵溶液,其他的常见不溶碱难溶于氯化铵.
③很多合金是金属互化物,有确定的化学组成.
④固体L与某种宝石的主要成分相同.
【探究思路】①确定焰火原料所含金属种类;②测定焰火原料的化学式.
【实验探究】
(1)甲同学进行了初步试验,实验步骤和实验现象如下.请填写下表.
(2)乙同学取甲第②组实验的溶液,加入镁试剂(Ⅰ)染料,得出合金中不含镁.乙的结论 (选填“正确”或“错误”).判断理由为 .
(3)丙同学设计实验方案,确定焰火原料中的金属种类,实验记录如下.
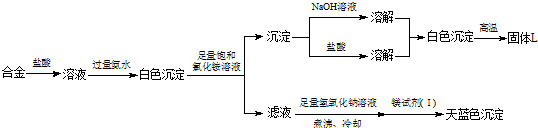
由丙的实验记录可知,该焰火原料是由 (填元素名称)两种金属组成的合金;实验中滤液加入足量氢氧化钠溶液后需煮沸,煮沸的理由是 .
(4)丁同学利用丙同学的结论,设计如下所示的实验步骤,确定合金组成.
 问题讨论:
问题讨论:
①能确定合金组成的数据组有 (填写选项字母);
a.m、n b.m、y c.n、y
②若合金中相对原子质量较小的金属的物质的量分数为x,金属总物质的量为7mol,试在如图中作出y随x变化的曲线;
③当y=8.5mol时,该合金是一种金属互化物,其化学式为 .
【探究目的】探究该焰火原料的组成
【资料检索】①Mg2+检验方法:取2滴待检液,加入2滴2mol?L-1 NaOH溶液,再加入1滴镁试剂(Ⅰ)染料(对硝基苯偶氮苯二酚).若出现沉淀并吸附镁试剂(Ⅰ)染料呈天蓝色,表示待检液中含有Mg2+.Ag+、Cu2+、Fe3+、NH4+会妨碍Mg2+检出.
②Mg(OH)2可溶于浓的氯化铵溶液,其他的常见不溶碱难溶于氯化铵.
③很多合金是金属互化物,有确定的化学组成.
④固体L与某种宝石的主要成分相同.
【探究思路】①确定焰火原料所含金属种类;②测定焰火原料的化学式.
【实验探究】
(1)甲同学进行了初步试验,实验步骤和实验现象如下.请填写下表.
| 试验序号 | 实 验 步 骤 | 实 验 现 象 | 结 论 |
| ① | 取少量该焰火原料加入冷水 | 无明显现象 | 不含有Li、Na等活泼金属 |
| ② | 取少量该焰火原料加入稀盐酸 | 完全溶解,有大量气体 |
(3)丙同学设计实验方案,确定焰火原料中的金属种类,实验记录如下.

由丙的实验记录可知,该焰火原料是由
(4)丁同学利用丙同学的结论,设计如下所示的实验步骤,确定合金组成.
 问题讨论:
问题讨论:①能确定合金组成的数据组有

a.m、n b.m、y c.n、y
②若合金中相对原子质量较小的金属的物质的量分数为x,金属总物质的量为7mol,试在如图中作出y随x变化的曲线;
③当y=8.5mol时,该合金是一种金属互化物,其化学式为
考点:探究物质的组成或测量物质的含量
专题:
分析:(1)①Na、Li等活泼金属和与水反应;
②能与盐酸反应为较活泼的金属;
(2)第②组实验所得的溶液含有过量盐酸,加入2滴NaOH溶液则不会产生沉淀;
(3)由题给信息可知Mg(OH)2可溶于浓的氯化铵溶液,应排除NH4+的干扰;
(4)①镁和铝都能与盐酸反应生成氢气,根据氢气的体积结合合金总质量可确定合金的组成,加入过量氢氧化钠得到的沉淀为氢氧化镁,灼烧后可得到氧化镁,根据氧化镁的质量可知镁的质量,则可知铝的质量;
②利用端值法判断;
③当y=8.5mol时,该合金是一种金属互化物,设合金中Mg为m mol,Al为n mol,则m+n=7 m+1.5n=8.5,解得m=4,n=3.
②能与盐酸反应为较活泼的金属;
(2)第②组实验所得的溶液含有过量盐酸,加入2滴NaOH溶液则不会产生沉淀;
(3)由题给信息可知Mg(OH)2可溶于浓的氯化铵溶液,应排除NH4+的干扰;
(4)①镁和铝都能与盐酸反应生成氢气,根据氢气的体积结合合金总质量可确定合金的组成,加入过量氢氧化钠得到的沉淀为氢氧化镁,灼烧后可得到氧化镁,根据氧化镁的质量可知镁的质量,则可知铝的质量;
②利用端值法判断;
③当y=8.5mol时,该合金是一种金属互化物,设合金中Mg为m mol,Al为n mol,则m+n=7 m+1.5n=8.5,解得m=4,n=3.
解答:
解:(1)①原料加入冷水无现象表明不含Li、Na等活泼金属;
②原料与盐酸反应产生气体表明含有能与盐酸反应的较活泼的金属,可能含铍(Be)、镁(Mg)、铝(Al)三种金属中的任意两种;
故答案为:可能含铍(Be)、镁(Mg)、铝(Al)三种金属中的任意两种;
(2)第②组实验所得的溶液含有过量盐酸,加入2滴NaOH溶液则不会产生沉淀,从而不能吸附镁试剂(I)染料呈天蓝色,由资料知,反应必须在碱性条件下进行;
故答案为:错误;由资料知,反应必须在碱性条件下进行;
(3)由图结合题意知该合金含镁、铝(不溶于足量饱和氯化铵溶液的白色沉淀既能溶液盐酸又能溶液氢氧化钠),由于Mg(OH)2可溶于浓的氯化铵溶液,因此用镁试剂(Ⅰ)染料检验Mg2+时要排除NH4+的干扰,所以滤液加入足量氢氧化钠溶液将NH4+转化为NH3,煮沸将氨气赶出,
故答案为:Mg和Al;将NH4+转化为NH3,煮沸促进氨气逸出,防止NH4+干扰Mg2+的检验;
(4)①镁和铝都能与盐酸反应生成氢气,根据氢气的体积结合合金总质量可确定合金的组成,加入过量氢氧化钠得到的沉淀为氢氧化镁,灼烧后可得到氧化镁,根据氧化镁的质量可知镁的质量,则可知铝的质量,已知镁的质量和镁铝生成氢气的体积可知铝的质量,则a、b、c都可测定合金的组成,
故答案为:a、b、c;
②若合金中相对原子质量较小的金属的物质的量分数为x,金属总物质的量为7mol,相对分子质量较小的为镁,如x=0,则全被为铝,7mol铝反应生成10.5mol氢气,如全被为镁,即x=7,则生成氢气7mol,则图象为 ,
,
故答案为: ;
;
③当y=8.5mol时,该合金是一种金属互化物,设合金中Mg为m mol,Al为n mol,则m+n=7 m+1.5n=8.5,解得m=4,n=3,
则化学式为Mg4Al3,
故答案为:Mg4Al3.
②原料与盐酸反应产生气体表明含有能与盐酸反应的较活泼的金属,可能含铍(Be)、镁(Mg)、铝(Al)三种金属中的任意两种;
故答案为:可能含铍(Be)、镁(Mg)、铝(Al)三种金属中的任意两种;
(2)第②组实验所得的溶液含有过量盐酸,加入2滴NaOH溶液则不会产生沉淀,从而不能吸附镁试剂(I)染料呈天蓝色,由资料知,反应必须在碱性条件下进行;
故答案为:错误;由资料知,反应必须在碱性条件下进行;
(3)由图结合题意知该合金含镁、铝(不溶于足量饱和氯化铵溶液的白色沉淀既能溶液盐酸又能溶液氢氧化钠),由于Mg(OH)2可溶于浓的氯化铵溶液,因此用镁试剂(Ⅰ)染料检验Mg2+时要排除NH4+的干扰,所以滤液加入足量氢氧化钠溶液将NH4+转化为NH3,煮沸将氨气赶出,
故答案为:Mg和Al;将NH4+转化为NH3,煮沸促进氨气逸出,防止NH4+干扰Mg2+的检验;
(4)①镁和铝都能与盐酸反应生成氢气,根据氢气的体积结合合金总质量可确定合金的组成,加入过量氢氧化钠得到的沉淀为氢氧化镁,灼烧后可得到氧化镁,根据氧化镁的质量可知镁的质量,则可知铝的质量,已知镁的质量和镁铝生成氢气的体积可知铝的质量,则a、b、c都可测定合金的组成,
故答案为:a、b、c;
②若合金中相对原子质量较小的金属的物质的量分数为x,金属总物质的量为7mol,相对分子质量较小的为镁,如x=0,则全被为铝,7mol铝反应生成10.5mol氢气,如全被为镁,即x=7,则生成氢气7mol,则图象为
 ,
,故答案为:
 ;
;③当y=8.5mol时,该合金是一种金属互化物,设合金中Mg为m mol,Al为n mol,则m+n=7 m+1.5n=8.5,解得m=4,n=3,
则化学式为Mg4Al3,
故答案为:Mg4Al3.
点评:本题考查物质含量的测定,侧重于考查学生的实验能力和分析能力,注意根据物质的性质进行判断,题目难度较大.

练习册系列答案
相关题目
安全教育是化学教育的重要内容.根据你掌握的知识判断,下列各项中符合安全操作要求的是( )
①在加油站内拨打手机
②在煤矿巷道内用明火照明
③闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔
④为了节约药品,锌与稀硫酸一开始反应,就做氢气点燃实验
⑤稀释浓硫酸时,沿烧杯内壁将浓硫酸缓缓加入水中,边加边搅拌
⑥不慎将酒精灯打翻在桌上失火时,立即用湿抹布盖灭
⑦不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛
⑧不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液.
①在加油站内拨打手机
②在煤矿巷道内用明火照明
③闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔
④为了节约药品,锌与稀硫酸一开始反应,就做氢气点燃实验
⑤稀释浓硫酸时,沿烧杯内壁将浓硫酸缓缓加入水中,边加边搅拌
⑥不慎将酒精灯打翻在桌上失火时,立即用湿抹布盖灭
⑦不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛
⑧不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液.
| A、③⑤⑥⑦⑧ | B、①②④ |
| C、①②⑥⑦⑧ | D、③④⑤⑦⑧ |
A、B、C、D 4种化合物,其焰色反应均为浅紫色,A、B、C和盐酸反应都可得到D;B、C 以等物质的量在溶液中反应可得到A;若在B溶液中通入一种无色无刺激性气味的气体,适量时得A,过量时得C,则A、B、C、D分别是( )
| A、KHCO3 KAlO2 K2CO3 KCl |
| B、K2CO3 KOH KHCO3 KCl |
| C、K2SO4 KOH KHSO4 KCl |
| D、K2CO3 K2SiO3 KOH KCl |



 与浓硫酸、浓硝酸混合在不同温度下会得到不同产物.
与浓硫酸、浓硝酸混合在不同温度下会得到不同产物.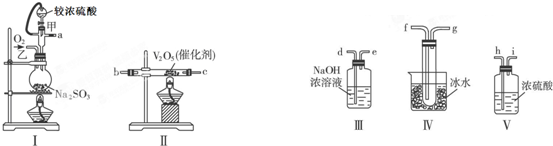
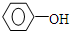 ;④CH3COOC2H5;⑤CH3COOH五物质中:
;④CH3COOC2H5;⑤CH3COOH五物质中: