题目内容
1.如图所示,将两烧杯中电极用导线相连.当闭合开关S后,以下表述正确的是( )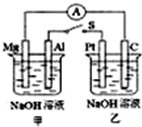
| A. | 电流表指针不发生偏转 | |
| B. | Al、Pt两极有H2产生 | |
| C. | Mg、C两极生成的气体可以恰好完全反应 | |
| D. | 甲池pH减小,乙池pH不变 |
分析 关闭开关S甲装置形成原电池反应,铝做负极失电子发生氧化反应,镁做正极,电极上得到电子发生还原反应,乙池为电解池,Pt做电解池阴极,C做电解池的阳极;
A.电流计有电流通过;
B.铝电极是原电池负极溶解无气体生成,Pt电极上氢离子得到电子生成氢气;
C.镁电极生成的氢气,C电极生成的是氧气;
D.甲装置是原电池消耗氢氧根离子,溶液PH减小;乙池是电解池,电极水溶液浓度增大,氢氧化钠溶液PH增大.
解答 解:关闭开关S甲装置形成原电池反应,铝做负极失电子发生氧化反应,镁做正极,电极上得到电子发生还原反应,乙池为电解池,Pt做电解池阴极,C做电解池的阳极;
A.甲装置形成的原电池,反应过程中有电子转移产生电流,电流计有电流通过,故A错误;
B.铝电极是原电池负极溶解无气体生成,Pt电极上氢离子得到电子生成氢气,故B错误;
C.镁电极生成的氢气,C电极生成的是氧气,依据电子守恒可知生成2mol氢气同时生成1mol氧气,氢气和氧气恰好反应生成水,故C正确;
D.甲装置是原电池消耗氢氧根离子,溶液pH减小;乙池是电解池,电极水溶液浓度增大,氢氧化钠溶液pH增大,故D错误;
故选C.
点评 本题考查原电池和电解池原理,为高频考点,侧重于学生的分析能力的考查,正确判断原电池和电解池及其正负极和阴阳极是解本题关键,明确离子的放电顺序,难度不大.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
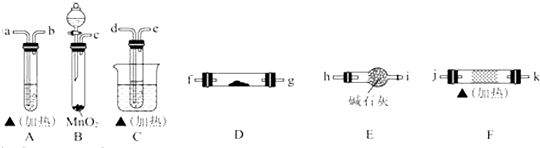
11.下列实验操作错误的是( )
| A. |  浓硫酸的稀释 | B. |  除去氯气中氯化氢 | ||
| C. |  碳酸、苯酚酸性强弱比较 | D. |  氯化氢气体的吸收 |
12.家用炒菜铁锅用水清洗放置后出现红棕色的锈斑,在此变化过程中不发生的化学反应是( )
| A. | 4Fe(OH)2+2H2O+O2═4Fe(OH)3 | B. | 2Fe+2H2O+O2═2Fe(OH)2 | ||
| C. | 2H2O+O2+4e-→4OH- | D. | Fe→Fe3++3e- |
16.下列说法正确的是( )
| A. |  如图研究的是温度、压强对平衡的影响,横坐标表示压强 | |
| B. |  如图研究的是温度对平衡的影响,Ⅱ采用的温度更高 | |
| C. |  图中t0时使用了催化剂,使平衡向正反应方向进行 | |
| D. |  图中t0时增大压强,使平衡向负反应方向进行 |
13.“试玉要烧三日满,辨材须待七年期”是唐代诗人白居易的名句,下列有关“玉”的说法正确的是( )
| A. | 玉是石灰石 | B. | 玉的硬度比河砂大 | ||
| C. | 玉的熔点较高 | D. | 玉是金刚砂 |
11.甲、乙、丙、丁4种无机化合物均含有2种元素,分子中均含18个电子.甲是气态氢化物,在水中分步电离出两种阴离子.下列推断合理的是( )
| A. | 某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 | |
| B. | 乙和甲中同种元素的质量分数相等,则乙能使湿润的KI淀粉试纸变蓝 | |
| C. | 丙中含有ⅣA族元素,则相同条件下丙比甲稳定 | |
| D. | 若丁分子空间构型为三角锥型,则丁分子间存在氢键 |
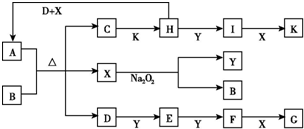 如图所示的转化关系中,已知A是由短周期元素组成的酸式盐.D、Y、H为气体,X为无色液体,G和K均是常见的强酸.H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,一个D分子中含有10个电子.试回答下列问题:
如图所示的转化关系中,已知A是由短周期元素组成的酸式盐.D、Y、H为气体,X为无色液体,G和K均是常见的强酸.H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,一个D分子中含有10个电子.试回答下列问题: