题目内容
在标况下,10克某气体中含有和11.2升CO2相等的分子数,则该气体的相对分子质量是( )
| A、20 | B、25 |
| C、40 | D、12.5 |
考点:摩尔质量,物质的量的相关计算
专题:阿伏加德罗常数和阿伏加德罗定律
分析:根据n=
计算二氧化碳的物质的量,通过M=
计算摩尔质量,摩尔质量在数值上等于相对分子质量.
| V |
| Vm |
| m |
| n |
解答:
解:标况下,Vm=22.4L/mol,n(CO2)=
=0.5mol,该气体与二氧化碳的分子数相同说明该气体的物质的量也为0.5mol,则该气体的摩尔质量M=
=
=20g/mol,因此该气体的相对分子质量为20,
故选A.
| 11.2L |
| 22.4L/mol |
| m |
| n |
| 10g |
| 0.5mol |
故选A.
点评:本题涉及物质的量的有关计算,难度不大,加强公式的综合应用和数据分析能力,注意摩尔质量以g/mol作单位时,数值上等于该物质的相对分子质量或相对原子质量.

练习册系列答案
相关题目
下列各组物质中,两种物质分子数相同的是( )
| A、1gH2和8gO2 |
| B、18gH2O和22.4LCO2(标准状况) |
| C、0.5molHCl和11.2LCO(20℃101kPa时) |
| D、6.02×1023个H2分子和0.5molN2 |
在实验室中,下列除去杂质的方法正确的是( )
| A、溴苯中混有溴,加入KI溶液,用汽油萃取 |
| B、乙烷中混有乙烯,通入氢气在一定条件下反应,使乙烯转化为乙烷 |
| C、硝基苯中混有浓硝酸和浓硫酸,将其倒入浓烧碱溶液中,静置,然后分液 |
| D、乙烷中混有乙炔,通入高锰酸钾酸性溶液洗气除去 |
下列叙述正确的是( )
| A、由两种元素构成的共价化合物分子中的化学键都是极性键 |
| B、含有非极性键的化合物不一定是共价化合物 |
| C、金属元素不可能存在于阴离子中 |
| D、离子化合物中一定含有金属元素 |
在周期表中存在对角线规则,据此判断下列物质的性质相似性的是( )
| A、氮和硅 | B、铝和铁 |
| C、铍和铝 | D、铜和金 |
下列粒子中核外未成对电子数目最多的是( )
| A、P |
| B、Fe3+ |
| C、Cr |
| D、Cu |
下列各组物质性质的比较中,正确的是( )
| A、热稳定性:NH3<PH3<H2O |
| B、酸性:H3PO4>H2SO4>HClO4 |
| C、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D、金属性:Na>Mg>Al |
如图所示的装置中,能够组成原电池,产生电流的是( )
A、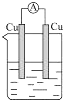 稀硫酸 |
B、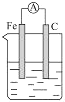 NaCl溶液 |
C、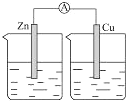 稀盐酸 |
D、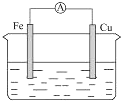 酒精 |