��Ŀ����
������һ����ı��أ���ˮ���̺�80����Ԫ�أ��ȼҵ���Ʊ�����þ��ԭ�϶������ں�ˮ��
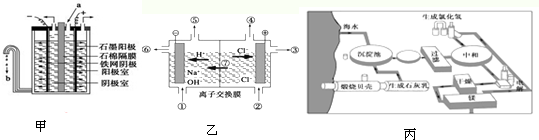
�����ȼҵ�У�����ʯ��Ĥ���������ʳ��ˮ����ͼ����ʾ����
��1��д�������ķ�Ӧʽ�� ��
��2��ͼ����������b�� ��Һ��
��3��ʯ��Ĥ�������� ��
�����ſƼ��ķ�չ�����ղ��ϸ��£����Ч�ʺͲ�Ʒ���ȵõ���ߣ�20����80����𣬸�Ĥ�����������ӽ���Ĥ��⼼��ȡ����
��1�����ӽ���Ĥ���ۣ���ͼ����ʾ���Тޡ��߷ֱ��� �� ��
��2����֪һ�����ӵĵ�����1.602��10-19C��������Ĥ���۵�ⱥ��ʳ��ˮ������·��ͨ��1.929��105 C�ĵ���ʱ������NaOH g��
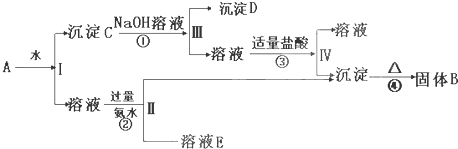
��ͼ���ǹ�ҵ������þ�����̣�
��1��д�����з�Ӧ�Ļ�ѧ����ʽ���ٳ����أ� �ڵ� �⣺
��2����������������ѭ��ʹ�õ������� ��
��3�����������Ȼ�þ�Ľᾧˮ����ʹ֮��ˮת��Ϊ��ˮ�Ȼ�þ��ע����� ��

�����ȼҵ�У�����ʯ��Ĥ���������ʳ��ˮ����ͼ����ʾ����
��1��д�������ķ�Ӧʽ��
��2��ͼ����������b��
��3��ʯ��Ĥ��������
�����ſƼ��ķ�չ�����ղ��ϸ��£����Ч�ʺͲ�Ʒ���ȵõ���ߣ�20����80����𣬸�Ĥ�����������ӽ���Ĥ��⼼��ȡ����
��1�����ӽ���Ĥ���ۣ���ͼ����ʾ���Тޡ��߷ֱ���
��2����֪һ�����ӵĵ�����1.602��10-19C��������Ĥ���۵�ⱥ��ʳ��ˮ������·��ͨ��1.929��105 C�ĵ���ʱ������NaOH
��ͼ���ǹ�ҵ������þ�����̣�
��1��д�����з�Ӧ�Ļ�ѧ����ʽ���ٳ����أ�
��2����������������ѭ��ʹ�õ�������
��3�����������Ȼ�þ�Ľᾧˮ����ʹ֮��ˮת��Ϊ��ˮ�Ȼ�þ��ע�����
���㣺���ԭ��,ԭ��غ͵��صĹ���ԭ��
ר�⣺�绯ѧר��
��������1�������������ӷŵ磻
��2�������������ӷŵ磬�����������������������ƣ�
��3��ʯ��Ĥ��������ֹ����ͨ����
��1������Ĥ����ֻ���������Ӻ�ˮ����ͨ����
��2��һ�����ӵĵ�����1.602��10-19C������·��ͨ��1.929��105 C�ĵ���ʱ�����ӵĸ���=
=1.204��1024�����ӵ����ʵ���=
=2mol������ת�Ƶ��Ӻ��������ƵĹ�ϵʽ���㣻
��1����������ĺ�ˮ�м���ʯ���飬���������ˡ�ϴ�ӳ�����õ�������þ�������������ֽⷴӦ�ڵ�������Ȼ�þ��Ϊ������ԭ��Ӧ������þ��������
��2����������ͼ���Կ�������������ѭ�����ã�
��3���Ȼ�þ�е�þ������ˮ�⣬�����Ի����¿�������ˮ�⣮
��2�������������ӷŵ磬�����������������������ƣ�
��3��ʯ��Ĥ��������ֹ����ͨ����
��1������Ĥ����ֻ���������Ӻ�ˮ����ͨ����
��2��һ�����ӵĵ�����1.602��10-19C������·��ͨ��1.929��105 C�ĵ���ʱ�����ӵĸ���=
| 1.929��105C |
| 1.602��10-19C |
| 1.204��1024 |
| 6.02��1023/mol |
��1����������ĺ�ˮ�м���ʯ���飬���������ˡ�ϴ�ӳ�����õ�������þ�������������ֽⷴӦ�ڵ�������Ȼ�þ��Ϊ������ԭ��Ӧ������þ��������
��2����������ͼ���Կ�������������ѭ�����ã�
��3���Ȼ�þ�е�þ������ˮ�⣬�����Ի����¿�������ˮ�⣮
���
�⣺��1�������������ӷŵ������������缫��ӦʽΪ��2Cl--2e-=Cl2����
�ʴ�Ϊ��2Cl--2e-=Cl2����
��2�������������ӷŵ磬����������������NaOH����Һ�л��в����Ȼ��ƣ�����b������Һ����NaOH��NaCl���ʴ�Ϊ��NaOH��NaCl��
��3��Cl2��NaOH��Һ�Ӵ���������Ӧ2NaOH+Cl2�TNaClO+NaCl+H2O����ֹCl2��NaOH��Ӧ��ʯ��Ĥ����������ֹ����ͨ����
�ʴ�Ϊ����ֹ����ͨ����
��1����ⱥ��ʳ��ˮ����������Ĥ�����������ӣ���Na+����ˮ����ͨ����������������ͨ���������������ӷŵ�����������ͬʱ�����������ƣ����Ԣ�Ϊ�������ƣ���ΪNa+��
�ʴ�Ϊ��NaOH��Һ��Na+��
��2��һ�����ӵĵ�����1.602��10-19C������·��ͨ��1.929��105 C�ĵ���ʱ�����ӵĸ���=
=1.204��1024��
���ӵ����ʵ���=
=2mol������ת�Ƶ��Ӻ��������ƵĹ�ϵʽ��NaOH������=
��2��40g/mol=80g��
�ʴ�Ϊ��80��
��1���ٰѺ�ˮ�е��Ȼ�þת����������þ������������ˮ�м���ʯ�ң��Ȼ�þ��ʯ����ijɷ��������Ʒ�ӦMgCl2+Ca��OH��2�TMg��OH��2+CaCl2������������þ������ˮ����˿��Բ��ù��˵ķ���ʹ���������������ʯ���������������������þ��������������
�ʴ�Ϊ��MgCl2+Ca��OH��2�TMg��OH��2+CaCl2��
����ˮ�Ȼ�þ������״̬�£�ͨ�����õ�����þ����ѧ����ʽΪ��MgCl2�����ڣ�
Mg+Cl2����
�ʴ�Ϊ��MgCl2�����ڣ�
Mg+Cl2����
��2����������ͼ���Կ�������������ѭ�����ã��ʴ�Ϊ����������Cl2����
��3���Ȼ�þ�е�þ������ˮ�⣬�ڸ����HCl�����У�������MgCl2ˮ�⣬�Ҵ���MgCl2?6H2O���Ȳ�����ˮ�����õ���ˮMgCl2��
�ʴ�Ϊ��Ϊ�˷�ֹ�Ȼ�þˮ�⣬Ҫ���Ȼ�������ķ�Χ�н��м��ȣ�
�ʴ�Ϊ��2Cl--2e-=Cl2����
��2�������������ӷŵ磬����������������NaOH����Һ�л��в����Ȼ��ƣ�����b������Һ����NaOH��NaCl���ʴ�Ϊ��NaOH��NaCl��
��3��Cl2��NaOH��Һ�Ӵ���������Ӧ2NaOH+Cl2�TNaClO+NaCl+H2O����ֹCl2��NaOH��Ӧ��ʯ��Ĥ����������ֹ����ͨ����
�ʴ�Ϊ����ֹ����ͨ����
��1����ⱥ��ʳ��ˮ����������Ĥ�����������ӣ���Na+����ˮ����ͨ����������������ͨ���������������ӷŵ�����������ͬʱ�����������ƣ����Ԣ�Ϊ�������ƣ���ΪNa+��
�ʴ�Ϊ��NaOH��Һ��Na+��
��2��һ�����ӵĵ�����1.602��10-19C������·��ͨ��1.929��105 C�ĵ���ʱ�����ӵĸ���=
| 1.929��105C |
| 1.602��10-19C |
���ӵ����ʵ���=
| 1.204��1024 |
| 6.02��1023/mol |
| 2mol |
| 2 |
�ʴ�Ϊ��80��
��1���ٰѺ�ˮ�е��Ȼ�þת����������þ������������ˮ�м���ʯ�ң��Ȼ�þ��ʯ����ijɷ��������Ʒ�ӦMgCl2+Ca��OH��2�TMg��OH��2+CaCl2������������þ������ˮ����˿��Բ��ù��˵ķ���ʹ���������������ʯ���������������������þ��������������
�ʴ�Ϊ��MgCl2+Ca��OH��2�TMg��OH��2+CaCl2��
����ˮ�Ȼ�þ������״̬�£�ͨ�����õ�����þ����ѧ����ʽΪ��MgCl2�����ڣ�
| ||
�ʴ�Ϊ��MgCl2�����ڣ�
| ||
��2����������ͼ���Կ�������������ѭ�����ã��ʴ�Ϊ����������Cl2����
��3���Ȼ�þ�е�þ������ˮ�⣬�ڸ����HCl�����У�������MgCl2ˮ�⣬�Ҵ���MgCl2?6H2O���Ȳ�����ˮ�����õ���ˮMgCl2��
�ʴ�Ϊ��Ϊ�˷�ֹ�Ȼ�þˮ�⣬Ҫ���Ȼ�������ķ�Χ�н��м��ȣ�
���������⿼�����ȼҵ��þ���Ʊ�����ȷ��Ӧԭ���ǽⱾ��ؼ�����Ϥ���ӽ�������ȡ�����������ķ�Ӧ��֪��þ��ұ��������ע���Ȼ�þ��ˮ�⣬Ϊ�״��㣮

��ϰ��ϵ�д�
�����Ŀ
��֪1g H2��ȫȼ������Һ̬ˮ�ų�a KJ�������������Ȼ�ѧ����ʽ��ȷ���ǣ�������
| A��H2 ��g��+1/2 O2��g��=H2O ��l����H=-a KJ��mol-1 |
| B��2H2��g��+O2��g��=2H2O��l����H=-4a KJ��mol-1 |
| C��2H2��g��+O2��g��=2H2O��l����H=+4a KJ��mol-1 |
| D��H2��g��+1/2 O2��g��=H2O��g����H=-2a KJ��mol-1 |
��֪���������Ȼ�ѧ����ʽ��
2H2��g��+O2��g��=2H2O��l����H=-571.6kJ/mol
CH4��g��+2O2��g��=2H2O��l��+CO2��g����H=-890.3kJ/mol
ʵ���������ͼ���Ļ�����干4mol����ȫȼ��ʱ����Ϊ2594kJ�����������������ͼ���������Ϊ��������
2H2��g��+O2��g��=2H2O��l����H=-571.6kJ/mol
CH4��g��+2O2��g��=2H2O��l��+CO2��g����H=-890.3kJ/mol
ʵ���������ͼ���Ļ�����干4mol����ȫȼ��ʱ����Ϊ2594kJ�����������������ͼ���������Ϊ��������
| A��3��5 | B��3��2 |
| C��2��3 | D��5��3 |
�ֱ���pH=2��pH=3�Ĵ�����Һ�к͵����ʵ����Ŀ��Լ���Һ���������ִ�����Һ������ֱ�ΪV1��V2��V1��V2�Ĺ�ϵ��ȷ���ǣ�������
| A��V2=10V1 |
| B��V1��10V2 |
| C��V2��10V1 |
| D��V2��10V1 |