题目内容
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:
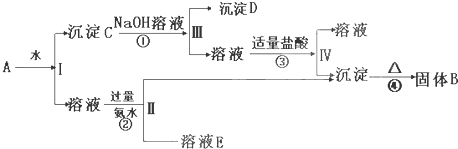
据此回答下列问题:
(1)I、Ⅱ、Ⅲ、Ⅳ四步中分离溶液和沉淀采用的相同的操作是 .
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式.固体B ;C ;沉淀D ;溶液E .
(3)写出①、③、④三个反应的化学方程式,②反应的离子方程式.
① ;② ;③ ;④ .
(4)若含KAl(SO4)2 0.15mol,同时将②氨水换成NaOH溶液,产生沉淀质量为7.8g,则需NaOH溶液的物质的量为 .

据此回答下列问题:
(1)I、Ⅱ、Ⅲ、Ⅳ四步中分离溶液和沉淀采用的相同的操作是
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式.固体B
(3)写出①、③、④三个反应的化学方程式,②反应的离子方程式.
①
(4)若含KAl(SO4)2 0.15mol,同时将②氨水换成NaOH溶液,产生沉淀质量为7.8g,则需NaOH溶液的物质的量为
考点:物质的分离、提纯的基本方法选择与应用
专题:实验设计题
分析:A溶于得到溶液和沉淀,Al2O3和Fe2O3不溶于水,所以C的成分是Al2O3和Fe2O3,向C中加入NaOH溶液,氧化铝和NaOH溶液反应生成NaAlO2,则D是Fe2O3,向滤液III中加入适量盐酸,偏铝酸钠和HCl反应生成NaCl和Al(OH)3,则沉淀是Al(OH)3,灼烧Al(OH)3得到Al2O3,所以固体B是Al2O3;
I滤液中含有KAl(SO4)2,KAl(SO4)2向中加入过量的氨水,二者反应生成氢氧化铝和K2SO4和(NH4)2SO4,所以溶液E中的溶质是K2SO4和(NH4)2SO4和NH3.H2O.
I滤液中含有KAl(SO4)2,KAl(SO4)2向中加入过量的氨水,二者反应生成氢氧化铝和K2SO4和(NH4)2SO4,所以溶液E中的溶质是K2SO4和(NH4)2SO4和NH3.H2O.
解答:
解:A溶于得到溶液和沉淀,Al2O3和Fe2O3不溶于水,所以C的成分是Al2O3和Fe2O3,向C中加入NaOH溶液,氧化铝和NaOH溶液反应生成NaAlO2,则D是Fe2O3,向滤液III中加入适量盐酸,偏铝酸钠和HCl反应生成NaCl和Al(OH)3,则沉淀是Al(OH)3,灼烧Al(OH)3得到Al2O3,所以固体B是Al2O3;
I滤液中含有KAl(SO4)2,KAl(SO4)2向中加入过量的氨水,二者反应生成氢氧化铝和K2SO4和(NH4)2SO4,所以溶液E中的溶质是K2SO4和(NH4)2SO4和NH3.H2O.
(1)I、Ⅱ、Ⅲ、Ⅳ四步中分离溶液和沉淀采用的相同的操作是过滤,故答案为:过滤;
(2)由以上分析可知B为Al2O3,C是Al2O3和Fe2O3,D为Fe2O3,E为K2SO4和(NH4)2SO4、NH3.H2O,
故答案为:Al2O3;Al2O3和Fe2O3;Fe2O3;K2SO4和(NH4)2SO4、NH3.H2O;
(3)反应①为Al2O3和氢氧化钠的反应,方程式为Al2O3+2NaOH=2NaAlO2+H2O,
反应②为Al3+和氨水的反应,反应的离子方程式为Al3++3NH3、H2O=Al(OH)3↓+3 NH4+,
反应③为偏铝酸钠和盐酸反应生成氢氧化铝沉淀的反应,反应的离子方程式为NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,
反应④为Al(OH)3的分解反应,方程式为2Al(OH)3
Al2O3+3H2O,
故答案为:Al2O3+2NaOH=2NaAlO2+H2O;Al3++3NH3?H2O=Al(OH)3↓+3NH4+;NaAlO2+HCl+H2O=Al(OH)3↓+NaCl;2Al(OH)3
Al2O3+3H2O;
(4)n(Al(OH)3)=
=0.1mol,若含KAl(SO4)2 0.15mol,说明铝元素部分转化为氢氧化铝,
如果NaOH溶液少量,则需要n(NaOH)=3n(Al(OH)3)=0.3mol,如果铝部分转化为氢氧化铝、部分转化为偏铝酸钠,则需要n(NaOH)=3n(Al(OH)3)+4n(NaAlO2)=0.3mol+4×0.05mol=0.5mol,
故答案为:0.3mol或0.5mol.
I滤液中含有KAl(SO4)2,KAl(SO4)2向中加入过量的氨水,二者反应生成氢氧化铝和K2SO4和(NH4)2SO4,所以溶液E中的溶质是K2SO4和(NH4)2SO4和NH3.H2O.
(1)I、Ⅱ、Ⅲ、Ⅳ四步中分离溶液和沉淀采用的相同的操作是过滤,故答案为:过滤;
(2)由以上分析可知B为Al2O3,C是Al2O3和Fe2O3,D为Fe2O3,E为K2SO4和(NH4)2SO4、NH3.H2O,
故答案为:Al2O3;Al2O3和Fe2O3;Fe2O3;K2SO4和(NH4)2SO4、NH3.H2O;
(3)反应①为Al2O3和氢氧化钠的反应,方程式为Al2O3+2NaOH=2NaAlO2+H2O,
反应②为Al3+和氨水的反应,反应的离子方程式为Al3++3NH3、H2O=Al(OH)3↓+3 NH4+,
反应③为偏铝酸钠和盐酸反应生成氢氧化铝沉淀的反应,反应的离子方程式为NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,
反应④为Al(OH)3的分解反应,方程式为2Al(OH)3
| ||
故答案为:Al2O3+2NaOH=2NaAlO2+H2O;Al3++3NH3?H2O=Al(OH)3↓+3NH4+;NaAlO2+HCl+H2O=Al(OH)3↓+NaCl;2Al(OH)3
| ||
(4)n(Al(OH)3)=
| 7.8g |
| 78g/mol |
如果NaOH溶液少量,则需要n(NaOH)=3n(Al(OH)3)=0.3mol,如果铝部分转化为氢氧化铝、部分转化为偏铝酸钠,则需要n(NaOH)=3n(Al(OH)3)+4n(NaAlO2)=0.3mol+4×0.05mol=0.5mol,
故答案为:0.3mol或0.5mol.
点评:本题考查了物质的分离和提纯,从整体上把握物质间的反应,明确物质的性质是解本题关键,知道流程图中每一步发生的反应,并能运用方程式表示,易错点是(4),注意:有两种情况,铝部分转化为氢氧化铝,一种情况是铝转化为氢氧化铝和偏铝酸钠.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、过量CO2通入澄清石灰水中:CO2+Ca2++2OH-=CaCO3↓+H2O |
| B、Na2O2与水发生反应:O22-+H2O=2OH-+H2↑ |
| C、向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-=Al(OH)3↓ |
| D、Ca(HCO3)2与足量的NaOH溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
下列变化过程中,需要吸收能量的是( )
| A、Cl2→Cl+Cl |
| B、H+Cl→HCl |
| C、C+O2→CO2 |
| D、H++OH-→H2O |
 已知A、J、D、E、G是元素周期表中1~36号元素,其原子序数依次增大.A与另外四种元素既不在同一周期,也不在同一主族.J和D同主族,E和G同周期;元素G是周期表中的第7列元素,E的最外层电子数与最内层电子数相同,E跟J可形成离子化合物,其晶胞结构(其中J原子在晶胞内部)如图.
已知A、J、D、E、G是元素周期表中1~36号元素,其原子序数依次增大.A与另外四种元素既不在同一周期,也不在同一主族.J和D同主族,E和G同周期;元素G是周期表中的第7列元素,E的最外层电子数与最内层电子数相同,E跟J可形成离子化合物,其晶胞结构(其中J原子在晶胞内部)如图.
