题目内容
由铜、锌和稀硫酸组成的原电池,在工作过程中,电解质溶液的pH( )
| A、逐渐变大 | B、先变小后变大 |
| C、逐渐变小 | D、不变 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:锌、铜和稀硫酸构成原电池,锌易失电子发生氧化反应而作负极,铜作正极,正极上氢离子得电子发生还原反应,根据溶液中氢离子浓度变化确定溶液酸碱性变化.
解答:
解:锌、铜和稀硫酸构成原电池,锌易失电子发生氧化反应而作负极,铜作正极,正极上氢离子得电子发生还原反应,所以电池反应式为Zn+2H+=H2↑+Zn2+,随着反应的进行,氢离子浓度逐渐减小,则溶液的酸性逐渐减小,pH将逐渐变大.
故选A.
故选A.
点评:本题考查了原电池原理,明确正负极上发生的反应及溶液酸性与氢离子浓度的关系是解本题关键,结合电池反应式来分析解答即可,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
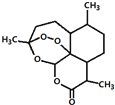 2011年9月23日,中国科学家屠呦呦获得了美国拉斯克医学奖的临床医学奖,获奖理由是“因为发现青蒿素--一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.如图是青蒿素的结构,则有关青蒿素的说法中不正确的是( )
2011年9月23日,中国科学家屠呦呦获得了美国拉斯克医学奖的临床医学奖,获奖理由是“因为发现青蒿素--一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.如图是青蒿素的结构,则有关青蒿素的说法中不正确的是( )| A、青蒿素分子式为C15H22O5 |
| B、青蒿素有-O-O-键具有较强的氧化性 |
| C、青蒿素易溶于水、乙醇、苯 |
| D、青蒿素在碱性条件下易发生水解反应 |
一定温度下,某密闭容器中发生如下反应:2X(g)+Y(s)?2Z(g),确实达到平衡的标志是( )
| A、X的生成速率与Z的消耗速率数值相等 |
| B、X、Y、Z的浓度之比为2:1:2 |
| C、体积一定时,容器内压强不再变化 |
| D、体积一定时,混合气体的密度不再变化 |
常温下,在溶液中可发生以下反应:①16H+10Z+2XO4-═2X+5Z2+8H2O,②2M+R2═2M+2R-,③2R-+Z2═R2+2Z-,由此判断下列说法错误的是( )
| A、Z元素在反应①中被氧化,在③中被还原 |
| B、还原性强弱顺序为:X2+<Z-<R-<M2+ |
| C、氧化性强弱顺序为:XO4-<Z2<R2<M |
| D、常温下不可发生反应2M2++Z2=2M3++2Z- |
下列有关物质保存的说法正确的组合是( )
①钠应该密封在煤油中保存;
②过氧化钠可以露置在空气中保存;
③氯水应该密封在无色试剂瓶中保存;
④漂白粉不能露置在空气中保存.
①钠应该密封在煤油中保存;
②过氧化钠可以露置在空气中保存;
③氯水应该密封在无色试剂瓶中保存;
④漂白粉不能露置在空气中保存.
| A、①③ | B、①④ |
| C、①③④ | D、①②③④ |
下列事实中,能说明氯的非金属性比硫强的是( )
| A、次氯酸的氧化性比稀硫酸强 |
| B、氯化氢比硫化氢的热稳定性好 |
| C、高氯酸(HClO4)的酸性比硫酸强 |
| D、氯原子最外层电子数比硫原子的多 |