题目内容
18.选择高效催化剂能使汽车尾气中NO、CO转化为N2和CO2,降低空气中污染性气体含量.(1)图1表示其他条件不变时,反应2CO(g)+2NO(g)?N2(g)+2CO2(g)中,c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线,已知催化剂表面积与化学反应速率成正比,不改变平衡体系中N2的体积分数.其他条件相同时,温度不同,化学反应限度不同.
①T1<(填“>”“<”或“=”)T2.
②在图象上画出温度为T2,接触面积为S2且S2<S1的曲线.
(2)在2L恒容密闭容器中充入2molNO和2molCO.实验测得NO转化为N2的转化率φ(NO)随温度变化曲线如图2,所示.
①若反应进行10min时到达A点,计算0~10min内用N2表示的化学反应速率c(N2)==0.04mol/L•min.
②在A点对应的容器中,混合气体压强与起始时的混合气体压强之比为4:5.
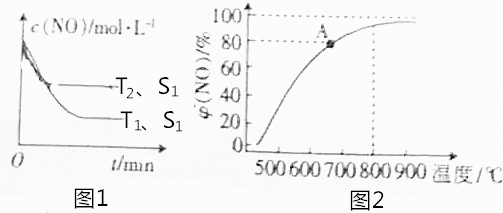
分析 (1)根据到达平衡的时间,判断温度高低,再根据不同温度下到达平衡时NO的浓度高低,判断温度对平衡的影响,据此判断反应热效应;催化剂的表面积S1>S2,则催化剂S1到达平衡的时间比催化剂S2短,催化剂不影响平衡移动,平衡时NO的浓度相同,据此作图;
(2)①若反应进行10min时到达A点,此时NO转化率为80%,则消耗NO物质的量=2mol×80%=1.6mol,依据化学方程式计算得到氮气生成物质的量为$\frac{1.6mol}{2}$=0.8mol,反应速率v=$\frac{△c}{△t}$;
②依据条件列出三行计算,气体压强之比等于化学方程式计量数之比;
解答 解:(1)①温度T2到达平衡的时间短,反应速率快,故温度T1<T2,
故答案为:<;
②温度越高,平衡时NO的浓度越高,说明升高温度平衡向逆反应移动,故正反应为放热反应,即△H<0;催化剂的表面积S1>S2,则催化剂S1到达平衡的时间比催化剂S2短,催化剂不影响平衡移动,平衡时NO的浓度相同,故c(NO) 在T2、S2条件下达到平衡过程中的变化曲线为: ,
,
故答案为: ;
;
(2)①若反应进行10min时到达A点,此时NO转化率为80%,则消耗NO物质的量=2mol×80%=1.6mol,依据化学方程式计算得到氮气生成物质的量为$\frac{1.6mol}{2}$=0.8mol,反应速率v=$\frac{△c}{△t}$=$\frac{\frac{0.8mol}{2L}}{10min}$=0.04mol/L•min,
故答案为:0.04mol/L•min;
②依据条件列出三行计算,
2CO(g)+2NO(g)?N2(g)+2CO2(g)
起始量(mol) 2 2 0 0
变化量(mol) 1.6 1.6 0.8 1.6
10min量(mol) 0.4 0.4 0.8 1.6
气体压强之比等于化学方程式计量数之比,
在A点对应的容器中,混合气体压强与起始时的混合气体压强之比=(0.4+0.4+0.8+1.6):(2+2)=4:5,
故答案为:4:5.
点评 本题考查了图象变化的分析判断,主要是化学平衡影响因素分析、化学反应速率的计算应用,注意气体压强之比等于气体物质的量之比,题目难度中等.

| A. | CH3CH(OH)CH3 | B. | CH3CH2CH2CH2OH | C. | CH3CH2CH2OH | D. | CH3CH2OCH2CH3 |
| A. | Li | B. | C | C. | Si | D. | S |
| A. | 可以确定该微粒为Ne | |
| B. | 对应元素的单质可能是强还原剂 | |
| C. | 对应元素可能是电负性最大的元素 | |
| D. | 对应元素可能位于元素周期表中第13列 |
| A. | σ键的特征是轴对称,π键的特征是镜面对称 | |
| B. | 气体单质中一定有σ键,可能有π键 | |
| C. | 乙烯与氢气发生加成反应时,乙烯分子中有π键断裂 | |
| D. | 当原子形成分子时,首先形成σ键,可能形成π键 |
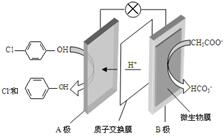 现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚,其原理如图所示,下列说法正确的是( )
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚,其原理如图所示,下列说法正确的是( )| A. | 电流方向从B极沿导线经小灯泡流向A极 | |
| B. | A极的电极反应式为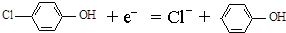 | |
| C. | 当外电路中有0.2mole-转移时,通过质子交换膜的H+的个数为0.2NA | |
| D. | B极为电池的正极,发生还原反应 |
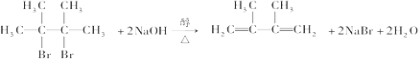 ;
;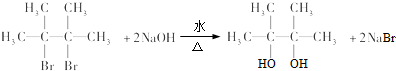 ;E与乙二醇的关系是同系物.
;E与乙二醇的关系是同系物. .
.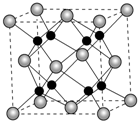 A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题: