题目内容
12.某同学欲用KMnO4固体配制100mL0.5mol.L-1的溶液.回答下列问题:(1)配制KMnO4溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、100mL容量瓶.
(2)应用托盘天平称取KMnO4固体7.9g.
(3)不规范的实验操作会导致实验结果的误差.分析下列操作对实验结果的影响偏小的是(请填序号)AD.
A.颠倒摇匀后发现凹液面低于刻度线又加水补上 B.加水定容时俯视刻度线
C.容量瓶内壁附有水珠而未干燥处理 D.在溶解过程中有少量液体溅出烧杯外.
分析 (1)依据配制一定物质的量浓度溶液步骤选择合适的仪器;
(2)依据m=CVM计算溶质的质量;
(3)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)配制一定物质的量浓度溶液步骤:计算、称量、溶解、移液、洗涤、定容、摇匀,用到的仪器为:托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、100mL容量瓶;
故答案为:胶头滴管;100mL容量瓶;
(2)配制100mL0.5mol.L-1的KMnO4溶液,需要溶质的质量=0.1L×0.5mol.L-1×158g/mol=7.9g;
故答案为:7.9g;
(3)A.颠倒摇匀后发现凹液面低于刻度线又加水补上,导致溶液体积偏大,溶液浓度偏低,故A正确;
B.加水定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故B错误;
C.容量瓶内壁附有水珠而未干燥处理,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故C错误;
D.在溶解过程中有少量液体溅出烧杯外,导致溶质的物质的量偏小,溶液浓度偏低,故D正确;
故选:AD.
点评 本题考查一定物质的量浓度溶液的配制,熟悉配制原理和过程是解题关键,题目难度不大,注意误差分析的方法.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
3.化学与日常生活紧密相关,下列说法错误的是( )
| A. | 氮肥NH4NO3在重力撞击下可能发生爆炸 | |
| B. | 在食品袋中放入盛有硅胶的透气小袋,可防止食物受潮 | |
| C. | 二氧化硅可用于制备太阳能电池板,晶体硅可用于制作光导纤维 | |
| D. | 碳酸氢钠可用来治疗胃酸过多 |
20.重金属离子Cu2+、Ba2+等均有毒.实验室有甲、乙两种废液,均有一定毒性.甲废液经化验呈碱性,主要有毒离子为Ba2+离子.如将甲、乙两废液按一定比例混合,毒性明显降低.乙废液中可能含有的离子是( )
| A. | Cu2+、Cl- | B. | Cu2+、SO42- | C. | Na+、SO42- | D. | Ag+、NO3- |
17.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.5mol O3的质量是16g | B. | 32gO2中含有的氧气分子数为2NA | ||
| C. | 1gH2中含有的电子数为NA | D. | 0.5NA个铜原子的质量为64g |
4.下列叙述正确的是(NA为阿伏加德罗常数的数值)( )
| A. | 22.4LCO2含有NA个CO2分子 | B. | 0.1NA个H2SO4分子的质量为9.8克 | ||
| C. | 10gCaCO3含有NA个C原子 | D. | 2molCl2含有2NA个Cl原子 |
1.下列各项反应对应的图象正确的是( )
| A. |  25℃时,向亚硫酸溶液中通入氯气 | B. |  向 Na[Al(OH)4]溶液中通入 HCl气体 | ||
| C. |  向少量氯化铁溶液中加入铁粉 | D. |  向BaSO4饱和溶液中加入硫酸钠 |
2.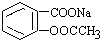 转变为
转变为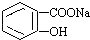 的方法是( )
的方法是( )
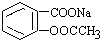 转变为
转变为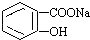 的方法是( )
的方法是( )| A. | 与足量Na0H溶液共热后,再通入CO2 | |
| B. | 溶液加热,通入足量的SO2 | |
| C. | 与稀硫酸共热后,加入足量Na0H溶液 | |
| D. | 足量稀硫酸共热后,加入足量NaHCO3 |
 制取 聚苯乙烯
制取 聚苯乙烯 .
. +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O.
+3H2O.