题目内容
6.下列有关 Na2CO3 和 NaHCO3 的说法错误的是( )| A. | 等质量 Na2CO3 和 NaHCO3 分别和足量盐酸反应,相同条件下前者生成 CO2 少 | |
| B. | 将石灰水分别加入 NaHCO3 和 Na2CO3 中,前者不生成沉淀 | |
| C. | 相同条件下 Na2CO3 比 NaHCO3 更易溶于水 | |
| D. | Na2CO3 固体中含少量 NaHCO3,可用加热法除去 |
分析 A.等质量的Na2CO3和NaHCO3,碳酸钠的摩尔质量大,其物质的量少;
B.Na2CO3和NaHCO3都能与澄清的石灰水反应生成沉淀;
C.相同条件下,碳酸铵的溶解度大于碳酸氢钠的溶解度;
D.NaHCO3不稳定,加热易分解.
解答 解:A.等质量的Na2CO3和NaHCO3,碳酸钠的摩尔质量大,其物质的量少,盐酸足量,碳元素守恒,则与盐酸完全反应碳酸钠产生的气体少,故A正确;
B.Na2CO3和NaHCO3都能与澄清的石灰水反应生成沉淀,反应为CO32-+Ca2+=CaCO3↓,2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32-,故B错误;
C.向饱和碳酸钠溶液中通入二氧化碳析出碳酸氢钠晶体,则相同条件下,在水中的溶解性为NaHCO3<Na2CO3,故C正确;
D.NaHCO3不稳定,加热易分解:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,碳酸钠受热稳定,可用加热法除去,故D正确;
故选B.
点评 本题考查碳酸钠和碳酸氢钠性质的比较,为高频考点,把握二者性质的差异是解答的关键,注意知识的积累和灵活应用,题目难度不大.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
17.下列反应中,△S<0的是( )
| A. | H2(g)+Br2(g)?2HBr(g) | B. | 2N2O5(g)=4NO2(g)+O2(g) | ||
| C. | 2SO2(g)+O2?2SO3(g) | D. | CaCO3(s)=CaO(s)+CO2(g) |
14.用O2将HCl转化为Cl2,反应方程式为:4HCl(g)+O2(g)?2H2O(g)+2Cl2(g)△H>0 一定条件下在1L密闭容器中测得反应过程中n(Cl2)的实验数据如表.下列说法正确的是( )
| t/min | 0 | 2 | 4 | 6 |
| n(Cl2)/10-3 mol | 0 | 1.8 | 3.7 | 5.4 |
| A. | 0~2 min的反应速率小于4~6 min的反应速率 | |
| B. | 2~6 min用Cl2表示的反应速率为0.9 mol/(L•min) | |
| C. | 降低温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动 | |
| D. | 平衡常数:K(200℃)<K(400℃) |
1.下列各物质中,所含分子数相同的是( )
| A. | 10gCH4和 10gO2 | B. | 11.2LN2(标准状况)和 11g CO2 | ||
| C. | 9 g H2O 和 0.5mol Cl2 | D. | 224mL H2(标准状况)和 0.1mol N2 |
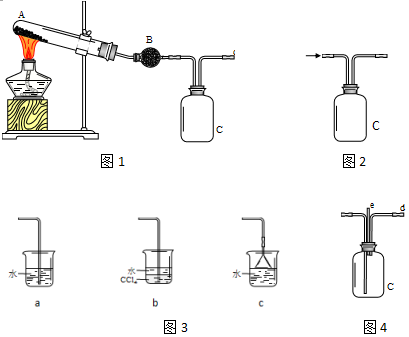
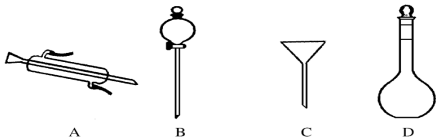
11.如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已 略).

(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.装置 B 中饱和食盐水的作用是;
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ依次放入④(填编号)
(3)装置 F 中用足量的 NaOH 溶液吸收余氯,试写出相应的离子方程式2OH-+Cl2=Cl-+ClO-+H2O.
(4)如果将二氧化锰与足量的浓盐酸混合加热,若有17.4g 的 MnO2 被还原,则被氧化的 HCl 的质量为7.3g.
(5)向 Na2CO3 溶液中通入氯气,可制得某种生产和生活中常用于漂白、消毒的 物质,同时有 NaHCO3 生成,该反应的化学方程式是2Na2CO3+Cl2+H2O=2NaHCO3+NaCl+NaClO.

(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.装置 B 中饱和食盐水的作用是;
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ依次放入④(填编号)
| ① | ② | ③ | ④ | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)如果将二氧化锰与足量的浓盐酸混合加热,若有17.4g 的 MnO2 被还原,则被氧化的 HCl 的质量为7.3g.
(5)向 Na2CO3 溶液中通入氯气,可制得某种生产和生活中常用于漂白、消毒的 物质,同时有 NaHCO3 生成,该反应的化学方程式是2Na2CO3+Cl2+H2O=2NaHCO3+NaCl+NaClO.
16.下列储存药品的方法中,正确的是( )
| A. | 液溴保存在带橡胶塞的玻璃瓶中 | |
| B. | 新制氯水保存在棕色广口瓶中 | |
| C. | 金属锂保存在石蜡油中 | |
| D. | 硅酸钠溶液保存在带磨口玻璃塞的玻璃瓶中 |