题目内容
(1)写出还原铁粉和水蒸气反应的化学方程式: .
(2)在进行焰色反应时用 溶液来洗涤铂丝(或光洁无锈铁丝).
(3)实验室制备氢氧化铝的最佳方案是向可溶性铝盐加入 溶液,离子方程式: .
(4)氢氧化亚铁的颜色为: .
(5)玛瑙的主要化学成分是: .
(6)王水是 和 以 比为 的混合溶液.
(7)当氯气和二氧化硫按照1:1的体积同时通入品红溶液中,观察到品红溶液没有明显变化,用化学方程式解释: .
(2)在进行焰色反应时用
(3)实验室制备氢氧化铝的最佳方案是向可溶性铝盐加入
(4)氢氧化亚铁的颜色为:
(5)玛瑙的主要化学成分是:
(6)王水是
(7)当氯气和二氧化硫按照1:1的体积同时通入品红溶液中,观察到品红溶液没有明显变化,用化学方程式解释:
考点:铁的化学性质,氯气的化学性质,焰色反应,镁、铝的重要化合物
专题:卤族元素,几种重要的金属及其化合物
分析:(1)铁与水蒸气反应生成四氧化三铁和氢气;
(2)盐酸洗涤,加热时挥发不干扰实验;
(3)氢氧化铝具有两性,但不能溶于弱碱溶液;
(4)氢氧化亚铁为白色不溶于水的固体;
(5)玛瑙的主要化学成分为二氧化硅;
(6)王水为浓盐酸与浓硝酸的混合物;
(7)氯气和二氧化硫按照1:1的体积同时通入品红溶液中,反应生成硫酸和盐酸,不具有漂白性.
(2)盐酸洗涤,加热时挥发不干扰实验;
(3)氢氧化铝具有两性,但不能溶于弱碱溶液;
(4)氢氧化亚铁为白色不溶于水的固体;
(5)玛瑙的主要化学成分为二氧化硅;
(6)王水为浓盐酸与浓硝酸的混合物;
(7)氯气和二氧化硫按照1:1的体积同时通入品红溶液中,反应生成硫酸和盐酸,不具有漂白性.
解答:
解:(1)铁与水蒸气反应生成四氧化三铁和氢气,化学反应为3Fe+4H2O(g)
Fe3O4+4H2,故答案为:3Fe+4H2O(g)
Fe3O4+4H2;
(2)盐酸洗涤,加热时挥发不干扰实验,则利用稀盐酸溶液来洗涤铂丝,故答案为:稀盐酸;
(3)氢氧化铝具有两性,但不能溶于弱碱溶液,则选择氨水与铝盐制备,离子反应为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故答案为:稀氨水;Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
(4)氢氧化亚铁为白色不溶于水的固体,故答案为:白色;
(5)玛瑙的主要化学成分为二氧化硅,其化学式为SiO2,故答案为:SiO2;
(6)王水为浓盐酸与浓硝酸的混合物,其体积比为3:1,故答案为:浓盐酸;浓硝酸;体积;3:1;
(7)氯气和二氧化硫按照1:1的体积同时通入品红溶液中,反应生成硫酸和盐酸,不具有漂白性,发生的反应为Cl2+SO2+2H2O=H2SO4+2HCl,
故答案为:Cl2+SO2+2H2O=H2SO4+2HCl.
| ||
| ||
(2)盐酸洗涤,加热时挥发不干扰实验,则利用稀盐酸溶液来洗涤铂丝,故答案为:稀盐酸;
(3)氢氧化铝具有两性,但不能溶于弱碱溶液,则选择氨水与铝盐制备,离子反应为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故答案为:稀氨水;Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
(4)氢氧化亚铁为白色不溶于水的固体,故答案为:白色;
(5)玛瑙的主要化学成分为二氧化硅,其化学式为SiO2,故答案为:SiO2;
(6)王水为浓盐酸与浓硝酸的混合物,其体积比为3:1,故答案为:浓盐酸;浓硝酸;体积;3:1;
(7)氯气和二氧化硫按照1:1的体积同时通入品红溶液中,反应生成硫酸和盐酸,不具有漂白性,发生的反应为Cl2+SO2+2H2O=H2SO4+2HCl,
故答案为:Cl2+SO2+2H2O=H2SO4+2HCl.
点评:本题考查常见物质的性质,为考试高频考点,注重于双基的考查,有利于培养学生的良好的科学素养,难度不大,注意相关基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某同学量取50ml 0.5mol/LNaOH溶液和30ml 0.5mol/L H2SO4溶液做中和热实验,测得中和热数据比57.3kJ?mol-1大,其原因可能是( )
| A、实验装置保温、隔热效果差 |
| B、量取NaOH溶液的体积时仰视读数 |
| C、分多次把NaOH溶液倒入盛有硫酸的小烧杯中 |
| D、用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 |
有关铝及其化合物的说法错误的是( )
| A、用于熔化烧碱的坩埚,可用Al2O3这种材料制成 |
| B、铝能在空气中稳定存在是因为其表面覆盖着一层氧化铝薄膜 |
| C、氧化铝是一种难熔物质,是一种较好的耐火材料 |
| D、氧化铝能中和胃酸,可用于制胃药 |
下列离子方程式书写正确的是( )
| A、向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -=2Al(OH)3↓+3BaSO4↓ |
| B、向FeI2溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl- |
| C、向Ba(OH)2溶液中加入过量的NaHCO3:Ba2++2OH-+2HCO3-=BaCO3↓+2H2O+CO32- |
| D、足量Cl2通入1.0mol?L-1 Na2SO3溶液中:2SO32-+Cl2=2S↓+2ClO3- |


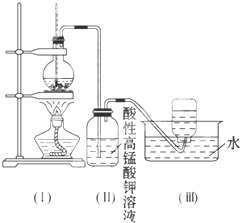 如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯:CH3CH2OH
如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯:CH3CH2OH ③CH3CH2OH ④CH3COOH ⑤聚乙烯五种物质中:
③CH3CH2OH ④CH3COOH ⑤聚乙烯五种物质中: