题目内容
有关铝及其化合物的说法错误的是( )
| A、用于熔化烧碱的坩埚,可用Al2O3这种材料制成 |
| B、铝能在空气中稳定存在是因为其表面覆盖着一层氧化铝薄膜 |
| C、氧化铝是一种难熔物质,是一种较好的耐火材料 |
| D、氧化铝能中和胃酸,可用于制胃药 |
考点:铝的化学性质,镁、铝的重要化合物
专题:几种重要的金属及其化合物
分析:A.Al2O3与NaOH反应;
B.氧化铝为致密的结构;
C.氧化铝的熔点高;
D.氧化铝与盐酸反应.
B.氧化铝为致密的结构;
C.氧化铝的熔点高;
D.氧化铝与盐酸反应.
解答:
解:A.Al2O3与NaOH反应,则用于熔化烧碱的坩埚,不能用Al2O3这种材料制成,应选铁坩埚,故A错误;
B.氧化铝为致密的结构,则铝能在空气中稳定存在,故B正确;
C.氧化铝的熔点高,则氧化铝是较好的耐火材料,故C正确;
D.氧化铝与盐酸反应,所以氧化铝能中和胃酸,可用于制胃药,故D正确;
故选A.
B.氧化铝为致密的结构,则铝能在空气中稳定存在,故B正确;
C.氧化铝的熔点高,则氧化铝是较好的耐火材料,故C正确;
D.氧化铝与盐酸反应,所以氧化铝能中和胃酸,可用于制胃药,故D正确;
故选A.
点评:本题考查Al及其化合物的性质,为高频考点,综合考查元素化合物知识,把握物质的性质及发生的反应为解答的关键,侧重分析与应用能力的考查,注意性质与用途的关系,题目难度不大.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
下面有关Na2CO3与NaHCO3的性质比较中错误的是( )
| A、热稳定性:Na2CO3>NaHCO3 |
| B、相同浓度溶液的碱性:Na2CO3>NaHCO3 |
| C、相同温度下在水中的溶解度:Na2CO3>NaHCO3 |
| D、相同条件下与酸反应的剧烈程度:Na2CO3>NaHCO3 |
常温下两种溶液:①1mol?L-1的Na2CO3溶液,②1mol?L-1的NaHCO3溶液.下列对于这两种溶液的说法正确的是( )
| A、两种溶液中都存在:c(H+)?c(OH-)═1×10-14 |
| B、c(H2CO3):①>② |
| C、两种溶液中都存在:c(Na+)+c(H+)═c(OH-)+c(HCO3-)+2c(CO32-) |
| D、向②溶液中加入等体积的1mol?L-1的NaOH溶液,②溶液可以变成①溶液 |
已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.30kJ?mol-1,在某温度下,2L的密闭容器中进行,测得如下数据:下列说法正确的是( )
 | 0 | 1 | 2 | 3 |
| N2 | 1.50 | n1 | 1.20 | n3 |
| H2 | 4.50 | 4.20 | 3.60 | n4 |
| NH3 | 0 | 0.20 | n2 | 1.00 |
| A、反应进行到1小时时放出的热量为9.23kJ |
| B、反应3h内,反应速率v(N2)为0.17mol?L-1?h-1 |
| C、此温度下,该反应的平衡常数为0.037 |
| D、4h时,若再加入1molN2,达到新的平衡时,N2的转化率是原来的两倍 |
下列与实验相关的叙述正确的是( )
| A、将FeCl3稀溶液加热蒸发浓缩制备FeCl3的浓溶液 |
| B、做氢气还原氧化铜的实验是,应先通氢气后加热氧化铜 |
| C、稀释浓硫酸时,应将蒸馏水沿烧杯内壁缓慢地注入浓硫酸中并不断搅拌 |
| D、配制1 mol?L-1350mLNaCl溶液可以选择一个100mL的容量瓶和一个250 mL的容量瓶 |
下列烷烃进行一氯取代反应后,生成三种沸点不同的产物的是( )
| A、(CH3)2CHCH2CH2CH3 |
| B、(CH3CH2)2CHCH3 |
| C、(CH3)3CCH2CH3 |
| D、(CH3)2CHCH(CH3)2 |
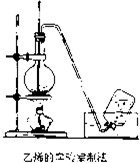 实验室制取乙烯的装置如图所示,请根据图示回答下列问题:
实验室制取乙烯的装置如图所示,请根据图示回答下列问题: