题目内容
已知醋酸、醋酸根离子在溶液中存在下列平衡:
CH3COOH+H2O 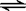 CH3COO—+H3O+
K1=1.75×10-5
CH3COO—+H3O+
K1=1.75×10-5
CH3COO—+H2O 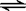 CH3COOH+OH—
K2=5.71×10-10
CH3COOH+OH—
K2=5.71×10-10
现有50 mL 0.2 mol·L-1醋酸与50 mL 0.2 mol·L-1醋酸钠混合制得溶液甲,下列叙述正确的是
A.甲溶液的pH >7
B.对甲进行微热,K1、K2同时增大
C.若在甲中加入很少量的NaOH溶液,溶液的pH几乎不变
D.若在甲中加入5 mL 0.1 mol·L-1的盐酸,则溶液中醋酸的K1会变大
【答案】
BC
【解析】
试题分析:A、K1大于K2,所以混合溶液中以醋酸的电离为主,溶液为酸性,错误;B、均为吸热反应,升高温度k值增大,正确;C、 若在甲中加入很少量的NaOH溶液,醋酸电离平衡正向移动,溶液的pH几乎不变,正确;D、温度不变,平衡常数不变,错误。
考点:考查溶液中的电离平衡有关问题。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
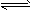 CH3COO-+H3O+ K1=1.75×10-5
CH3COO-+H3O+ K1=1.75×10-5 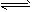 CH3COOH+OH- K2 =5.71×10-10
CH3COOH+OH- K2 =5.71×10-10