题目内容
5.地表水和地下水都来源于大气降水,但重水和轻水中同位素含量是不同的,有时差别还相当大,氢包括两种稳定核素:H和D,氧常见的核素16O、17O和18O,下列有关说法正确的是( )| A. | H2和D2互为同分异构体,其化学性质完全相同 | |
| B. | 电解一定量的D${\;}_{2}^{18}$O时,阴、阳两极所得气体的质量之比约为2:9 | |
| C. | 18O2和18O3互为同素异形体,其密度之比为2:3 | |
| D. | H${\;}_{2}^{16}$O、H${\;}_{2}^{17}$O、H${\;}_{2}^{18}$O互为同位素,都能与金属钠发生反应 |
分析 A、H2和D2为同元素形成的结构相同的单质,不互为同分异构体;
B、当电解1mol的D${\;}_{2}^{18}$O时阴极产生2molD2,阳极产生1mol氧气,据此分析计算;
C、相同状况下密度比等于摩尔质量之比;
D、同位素研究的对象为同元素的不同原子.
解答 解:A、H2和D2为同元素形成的结构相同的单质,不互为同分异构体,故A错误;
B、当电解1mol的D${\;}_{2}^{18}$O时阴极产生2molD2,阳极产生1mol18O2,阴、阳两极所得气体的质量之比为8:36=2:9,故B正确;
C、相同状况下密度比等于摩尔质量之比,题目中未说明相同状况,无法计算,故C错误;
D、同位素研究的对象为同元素的不同原子,H${\;}_{2}^{16}$O、H${\;}_{2}^{17}$O、H${\;}_{2}^{18}$O不能互为同位素,故D错误.
故选B.
点评 本题考查了同分异构体、同位素、同素异形体等基本概念,要求学生掌握基础知识,能够运用概念进行辨析和计算,难度不大.

练习册系列答案
相关题目
15.下列化学用语的表达方式不正确的是( )
①乙酸乙酯的结构简式:CH3CH2COOCH2CH3
②CO2分子的结构式:O=C=O
③乙烯的实验式:CH2
④S原子的结构示意图: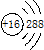
⑤葡萄糖结构简式:C6H12O6
⑥CH4Si的结构式:
①乙酸乙酯的结构简式:CH3CH2COOCH2CH3
②CO2分子的结构式:O=C=O
③乙烯的实验式:CH2
④S原子的结构示意图:
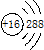
⑤葡萄糖结构简式:C6H12O6
⑥CH4Si的结构式:

| A. | 只有②⑤⑥ | B. | 只有①④⑤ | C. | 只有⑤⑥ | D. | 只有①②⑥ |
20.现有部分短周期元素的性质或原子结构如表:
(1)元素Z形成的单质电子式 ;
;
(2)Y的最高价氧化物与强碱反应的离子方程式Al2O3+2OH-+3H2O=2[Al(OH)4]-;
(3)元素X与元素T的非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是c(填字母);
a.X的氢化物比T的氢化物稳定
b.常温下X的单质和T的单质状态不同
c.T的单质能把X从其氢化物中置换出来
d..最高价氧化物的水化物的酸性X>T.
| 元素编号 | 元素性质或原子结构 |
| X | M层的电子数是原子核外电子层数的2倍 |
| Y | 最高价氧化物既能与强酸反应,又能与强碱反应 |
| Z | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| T | 最高价氧化物的水化物为无机酸中最强的酸 |
 ;
;(2)Y的最高价氧化物与强碱反应的离子方程式Al2O3+2OH-+3H2O=2[Al(OH)4]-;
(3)元素X与元素T的非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是c(填字母);
a.X的氢化物比T的氢化物稳定
b.常温下X的单质和T的单质状态不同
c.T的单质能把X从其氢化物中置换出来
d..最高价氧化物的水化物的酸性X>T.
10.氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是( )
| A. | 在相同条件下,HCN溶液的导电性比强酸溶液的弱 | |
| B. | HCN易溶于水 | |
| C. | 10 mL1mol/LHCN恰好与10 mL 1mol/L NaOH溶液完全反应 | |
| D. | 1mol/L氢氰酸溶液的pH约为3 |
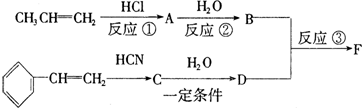
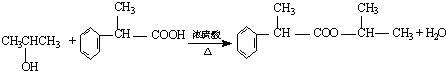
17.有机化学中取代反应范畴很广,下列4个反应中,属于取代反应范畴的是( )
| A. | 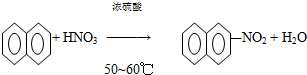 | |
| B. | CH3CH2CH2CHOHCH3$→_{△}^{浓硫酸}$CH3CH2CH=CHCH3+H2O | |
| C. | CH3CHO+H2$→_{催化剂}^{高温高压}$CH3CH2OH | |
| D. | 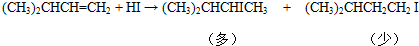 |
14.某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)
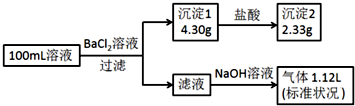
下列说法正确的是( )

下列说法正确的是( )
| A. | 原溶液中c(Cl-)≥0.1mol•L-1 | |
| B. | 取滤液,加硝酸银溶液,若产生白色沉淀,证明原溶液中存在Cl- | |
| C. | 原溶液一定存在CO32-和SO42-,一定不存在Na+ | |
| D. | 原溶液可能存在Cl-,不存在Fe3+ |
15.化学式为C4H8O3的有机物,在浓硫酸存在和加热时,有如下性质:
①能分别与CH3CH2OH和CH3COOH反应;
②脱水生成一种能使溴水褪色的物质,此物质只存在一种结构简式;
③能生成一种分子式为C4H6O2的五元环状化合物.
则C4H8O3的结构简式为( )
①能分别与CH3CH2OH和CH3COOH反应;
②脱水生成一种能使溴水褪色的物质,此物质只存在一种结构简式;
③能生成一种分子式为C4H6O2的五元环状化合物.
则C4H8O3的结构简式为( )
| A. | HOCH2CH2CH2COOH | B. | CH3CH(OH)CH2COOH | C. | HOCH2COOCH2CH3 | D. | CH3CH2CH(OH)COOH |
 .
. .
.