��Ŀ����
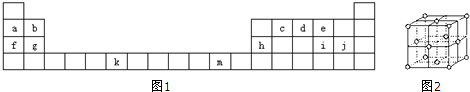
��һ���������ܱ������г���2mol A��0.6mol C��һ������B�������壬һ�������·�����Ӧ2A��g��+B��g��?3c��g���������ʵ�Ũ����ʱ��仯�Ĺ�ϵ��ͼ1��ʾ��������t0��t1��c��B��δ������ͼ2Ϊ��Ӧ��ϵ�з�Ӧ������ʱ��仯���������t2��t3��t4���ı�һ�ֲ�ͬ��������
��1����t1=15min����t0��t1����c��Ũ�ȱ仯��ʾ�ķ�Ӧ����V��C��= ��
��2��t3ʱ�ı������Ϊ ��B����ʼ���ʵ���Ϊ ��
��3��t4��t5�Σ���A�����ʵ���������O��01mol�����˽��з�Ӧ��ϵ��������Ϊa kJ��д���������¸÷�Ӧ���Ȼ�ѧ����ʽ�� ��

��1����t1=15min����t0��t1����c��Ũ�ȱ仯��ʾ�ķ�Ӧ����V��C��=
��2��t3ʱ�ı������Ϊ
��3��t4��t5�Σ���A�����ʵ���������O��01mol�����˽��з�Ӧ��ϵ��������Ϊa kJ��д���������¸÷�Ӧ���Ȼ�ѧ����ʽ��
���㣺���ʵ�����Ũ����ʱ��ı仯����,��ѧ��Ӧ�����뻯ѧƽ��ͼ����ۺ�Ӧ��
ר�⣺��ѧƽ��ר��
��������1��t0��t1����c��Ũ�ȱ仯��ʾ�ķ�Ӧ����V��C��=
����C���ʷ�Ӧ���ʣ�
��2���÷�Ӧ�ķ�Ӧǰ������������䣬t3ʱ�ı�������Ӧ���ʽ��ͣ�ƽ�ⲻ�ƶ����ı������Ǽ�Сѹǿ��ȡ�����ֻ�����壻ͬһ���淴Ӧͬһʱ����ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ��ݴ˼���B��ƽ����Ӧ���ʣ�����n=v��TV����μӷ�Ӧ��B�����ʵ�����
��3��t4��t5�Σ���A�����ʵ���������O��01mol�����˽��з�Ӧ��ϵ��������Ϊa kJ����μӷ�Ӧ��A�����ʵ���Ϊ2molʱ��������Ϊ200kJ���ݴ���д�Ȼ�ѧ��Ӧ����ʽ��
| ��C |
| ��t |
��2���÷�Ӧ�ķ�Ӧǰ������������䣬t3ʱ�ı�������Ӧ���ʽ��ͣ�ƽ�ⲻ�ƶ����ı������Ǽ�Сѹǿ��ȡ�����ֻ�����壻ͬһ���淴Ӧͬһʱ����ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ��ݴ˼���B��ƽ����Ӧ���ʣ�����n=v��TV����μӷ�Ӧ��B�����ʵ�����
��3��t4��t5�Σ���A�����ʵ���������O��01mol�����˽��з�Ӧ��ϵ��������Ϊa kJ����μӷ�Ӧ��A�����ʵ���Ϊ2molʱ��������Ϊ200kJ���ݴ���д�Ȼ�ѧ��Ӧ����ʽ��
���
�⣺��1��t0��t1����c��Ũ�ȱ仯��ʾ�ķ�Ӧ����v��C��=
=
mol/��L��min��=0.02mol/��L��min�����ʴ�Ϊ��0.02 mol/��L?min����
��2���÷�Ӧ�ķ�Ӧǰ������������䣬t3ʱ�ı�������Ӧ���ʽ��ͣ�ƽ�ⲻ�ƶ����ı������Ǽ�Сѹǿ��Ҳ����ȡ������ƽ�������壬��ƽ�ⲻ�ƶ����ҷ�Ӧ���ʽ��ͣ�
ͬһ���淴Ӧͬһʱ����ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ���B�ķ�Ӧ����=
v(C)=
��0.02mol/��L��min������Ӧ��ʼʱA�����ʵ���Ϊ2mol����Ũ��Ϊ1.0mol/L�����������Ϊ2L��
�μӷ�Ӧ��B�����ʵ���n=v��TV=
v(C)=
��0.02mol/��L��min����15min��2L=0.2mol��ƽ��ʱB�����ʵ���=0.4mol/L��2L=0.8mol����B�����ʵ���=0.2mol+0.8mol=1.0mol��
�ʴ�Ϊ����Сѹǿ��ȡ������ƽ�������壻1��O mol
��3��t4��t5�Σ���A�����ʵ���������O��01mol�����˽��з�Ӧ��ϵ��������Ϊa kJ����μӷ�Ӧ��A�����ʵ���Ϊ2molʱ��������Ϊ200kJ�����Ȼ�ѧ��Ӧ����ʽΪ2A��g��+B��g��?3C��g����H=+200a KJ/mol���ʴ�Ϊ��2A��g��+B��g��?3C��g����H=+200a KJ/mol��
| ��C |
| ��t |
| 0.6-0.3 |
| 15 |
��2���÷�Ӧ�ķ�Ӧǰ������������䣬t3ʱ�ı�������Ӧ���ʽ��ͣ�ƽ�ⲻ�ƶ����ı������Ǽ�Сѹǿ��Ҳ����ȡ������ƽ�������壬��ƽ�ⲻ�ƶ����ҷ�Ӧ���ʽ��ͣ�
ͬһ���淴Ӧͬһʱ����ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ���B�ķ�Ӧ����=
| 1 |
| 3 |
| 1 |
| 3 |
�μӷ�Ӧ��B�����ʵ���n=v��TV=
| 1 |
| 3 |
| 1 |
| 3 |
�ʴ�Ϊ����Сѹǿ��ȡ������ƽ�������壻1��O mol
��3��t4��t5�Σ���A�����ʵ���������O��01mol�����˽��з�Ӧ��ϵ��������Ϊa kJ����μӷ�Ӧ��A�����ʵ���Ϊ2molʱ��������Ϊ200kJ�����Ȼ�ѧ��Ӧ����ʽΪ2A��g��+B��g��?3C��g����H=+200a KJ/mol���ʴ�Ϊ��2A��g��+B��g��?3C��g����H=+200a KJ/mol��
���������⿼�黯ѧƽ��ļ��㣬�����ͼ���з�Ӧ������ʱ��仯ȷ���ı��������֪����ѧ��Ӧ���ʵ�Ӱ�����أ�֪����������ļ��㷽����Ϊ�״��㣮

��ϰ��ϵ�д�
�����Ŀ
ʵ������Ҫ����2mol/l��NaCl��Һ450ml������ʱӦѡ�õ�����ƿ�Ĺ��ͳ�ȡ��NaCl�����ֱ��ǣ�������
| A��450ml��52.65g |
| B��������52.65g |
| C��500 ml��58.5g |
| D��1000 ml��117g |
һ���¶��£����ڷ�ӦN2+O2?2NO���ܱ������н��У����д�ʩ�ܼӿ췴Ӧ���ʵ��ǣ�������
| A���ı��¶� |
| B�����ݣ�����N2 |
| C�����ݣ�����He�� |
| D����ѹ������He�� |
pH=1������һԪ��HX��HY��Һ���ֱ�ȡ50mL����������þ�ۣ���ַ�Ӧ���ռ���H2����ֱ�ΪV��HX����V��HY������V��HX����V��HY����������˵����ȷ���ǣ�������
| A��HX������ǿ�� |
| B��HX�����Ա�HY�������� |
| C�������Ũ�ȴ�С[HX]��[HY] |
| D��pH=1������һԪ���ϡ��100����ϡ�ͺ�����Һ��pH��Ϊ3 |
��1L����0.4molCuSO4��0.1molNaCl��ˮ��Һ�ö��Ե缫��⣬���һ��ʱ�����һ���缫�ϵõ�0.25molCu����һ���缫�ϲ������壨�����������ǣ�������
| A��4.48L |
| B��3.36L |
| C��6.72L |
| D��13.44L |
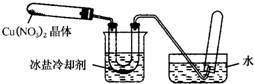 ij��ѧ̽��С������ͭƬ��ȡCu��NO3��2����̽���仯ѧ���ʣ�
ij��ѧ̽��С������ͭƬ��ȡCu��NO3��2����̽���仯ѧ���ʣ�