题目内容
由钠和铝构成的合金共 m g,放入适量水中充分反应(没有固体剩余)共产生 n L(标况)气体,试求合金中钠和铝的质量各是多少克?
考点:化学方程式的有关计算
专题:计算题
分析:根据钠与水发生反应:2Na+2H2O═2NaOH+H2↑,铝与氢氧化钠的发生反应:2Al+2NaOH+6H2O═2 Na[Al(OH)4]+3 H2↑,设该合金中钠和铝的质量分别为:xg、yg,表示出生成氢气的体积,根据二者质量及生成氢气的体积列方程计算解答.
解答:
解:设该合金中钠和铝的质量分别为:m(Na)、m(Al),
2Na+2H2O═2NaOH+H2↑
46g 22.4L
xg
=
L
2Al+2NaOH+6H2O═2 Na[Al(OH)4]+3 H2↑
54g 67.2L
yg
=
L
由题意可知:x+y=m
+
=n
解得x=
-
y=
-
答:合金中钠的质量为(
-
) g,合金中铝的质量(
-
) g.
2Na+2H2O═2NaOH+H2↑
46g 22.4L
xg
| xg×22.4L |
| 46g |
| 11.2x |
| 23 |
2Al+2NaOH+6H2O═2 Na[Al(OH)4]+3 H2↑
54g 67.2L
yg
| yg×67.2L |
| 54g |
| 11.2y |
| 9 |
由题意可知:x+y=m
| 11.2x |
| 23 |
| 11.2y |
| 9 |
解得x=
| 23m |
| 14 |
| 207n |
| 14×11.2 |
y=
| 207n |
| 14×11.2 |
| 9m |
| 14 |
答:合金中钠的质量为(
| 23m |
| 14 |
| 207n |
| 14×11.2 |
| 207n |
| 14×11.2 |
| 9m |
| 14 |
点评:本题考查混合物有关计算,难度中等,属于字母型计算,增大计算难度,为易错题目,侧重对基础知识的巩固,注意掌握根据方程式的计算.

练习册系列答案
相关题目
下列各组物质中,都是共价化合物的是( )
| A、H2S和Na2O2 |
| B、H2O2和CaF2 |
| C、NH3和N2 |
| D、HNO3和HClO3 |
“纳米材料”(1nm=10-9m)已广泛应用于催化及军事科学中.“纳米材料”是指研究开发直径为几纳米至几十纳米的材料,如将“纳米材料”分散到液体分散剂中.有以下叙述:①所得物质一定是溶液,②能全部透过半透膜,③有丁达尔现象,④所得液体可以全部透过滤纸.对所得分散系的上述叙述正确的是( )
| A、①② | B、②③ | C、①④ | D、③④ |
在标准状况下,A L NH3溶于B mL水中,得到密度为ρg/cm3的R L氨水,则此氨水的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列说法正确的是( )
A、NaHCO3溶液加水稀释,
| ||
| B、1 mol?L-1的NH4Cl溶液中含有NH4+的数目一定小于NA | ||
| C、用石墨电极电解FeCl3溶液,阴极反应:2Fe3++6H2O+6e-═2Fe(OH)3↓+3H2↑ | ||
| D、将带有相反电荷的胶体混合,一定会出现胶体聚沉现象 |
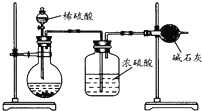 为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案: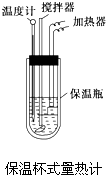 在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.