题目内容
请利用下列装置及试剂组装一套装置.其流程是,先制取纯净干燥的Cl2(不收集),后试验干燥的Cl2和潮湿的Cl2有无漂白性.
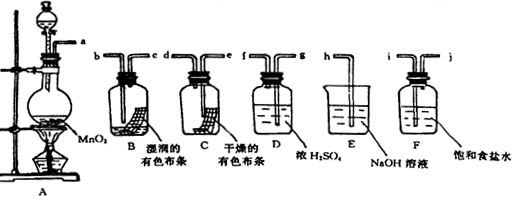
(1)按气体从左向右流向将各装置依次连接起来(填字母序号):a接 接 接 接 接h.
(2)A装置发生的化学反应方程式为 .
(3)E装置发生反应的离子方程式是: .
(4)C瓶中的现象是 ,B瓶中的现象是 .以上事实说明起漂白作用的物质是 .
(5)若将Cl2和SO2等物质的量混合漂白作用减弱,用化学方程式解释原因 .

(1)按气体从左向右流向将各装置依次连接起来(填字母序号):a接
(2)A装置发生的化学反应方程式为
(3)E装置发生反应的离子方程式是:
(4)C瓶中的现象是
(5)若将Cl2和SO2等物质的量混合漂白作用减弱,用化学方程式解释原因
考点:氯气的实验室制法,氯气的化学性质
专题:卤族元素
分析:(1)根据实验发生装置→除杂装置→性质检验装置→尾气处理装置排序解答;
(2)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水;
(3)氯气与氢氧化钠反应生成氯化钠、次氯酸钠、和水;
(4)氯气不具有漂白性,次氯酸具有漂白性;
(5)氯气具有强的氧化性能够与二氧化硫发生氧化还原反应,生成硫酸和氯化氢.
(2)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水;
(3)氯气与氢氧化钠反应生成氯化钠、次氯酸钠、和水;
(4)氯气不具有漂白性,次氯酸具有漂白性;
(5)氯气具有强的氧化性能够与二氧化硫发生氧化还原反应,生成硫酸和氯化氢.
解答:
解:(1)验装置的连接顺序为:发生装置→除杂装置→性质检验装置→尾气处理装置;因为收集的是气体,所以除杂装置中长导管进气,段导管出气;因为饱和食盐水中有水,浓硫酸有吸水性,所以先连接饱和食盐水装置后连接浓硫酸装置;试验干燥的Cl2和潮湿的Cl2有无漂白性,因为湿润的有色布条有水分,所以D装置先连接C后连接B;
故答案为:i j;g f;e d; b c;
(2)浓盐酸有还原性,二氧化锰有氧化性,浓盐酸和二氧化锰能发生氧化还原反应生成氯化锰、氯气和水,化学方程式为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(3)氯气与氢氧化钠反应生成氯化钠、次氯酸钠、和水,离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(4)氯气不具有漂白性,次氯酸具有漂白性,所以B中有色布条不褪色,C中有色布条褪色,故答案为:有色布条不褪色;有色布条褪色;次氯酸(HClO);
(5)氯气具有强的氧化性能够与二氧化硫发生氧化还原反应,生成硫酸和氯化氢,硫酸和氯化氢都不具有漂白性,故答案为:Cl2+SO2+2H2O=H2SO4+2HCl.
故答案为:i j;g f;e d; b c;
(2)浓盐酸有还原性,二氧化锰有氧化性,浓盐酸和二氧化锰能发生氧化还原反应生成氯化锰、氯气和水,化学方程式为MnO2+4HCl(浓)
| ||
故答案为:MnO2+4HCl(浓)
| ||
(3)氯气与氢氧化钠反应生成氯化钠、次氯酸钠、和水,离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(4)氯气不具有漂白性,次氯酸具有漂白性,所以B中有色布条不褪色,C中有色布条褪色,故答案为:有色布条不褪色;有色布条褪色;次氯酸(HClO);
(5)氯气具有强的氧化性能够与二氧化硫发生氧化还原反应,生成硫酸和氯化氢,硫酸和氯化氢都不具有漂白性,故答案为:Cl2+SO2+2H2O=H2SO4+2HCl.
点评:本题考查了氯气的实验室制法及其性质的检验,题目难度不大,明确反应的原理和氯气的性质、各装置的作用是解题关键,注意氯气不具有漂白性.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
下列表述中正确的是( )
| A、金属易锈蚀能用金属的电子气理论加以解释 |
| B、化学式Si02能真实表示物质分子组成 |
| C、共价键、离子键和范德华力都是微粒之间的不同作用力,Na2O2、石墨、白磷均含有上述两种作用力 |
| D、CCl4与KCl晶体中,化学键种类相同,晶体类型也相同 |
由(NH4)2SO4和MgSO4组成的混合物共192g,溶于水中配成10L溶液.测得此溶液中SO42-的物质的量浓度为0.15mol/L,则原混合物中NH4+的物质的量是( )
| A、0.1mol |
| B、0.5mol |
| C、1mol |
| D、2mol |
配制一定物质量浓度的NaOH溶液时,下列事实中一定会使配成溶液的实际浓度的实际浓度比所要求的浓度偏小的是( )
| A、用部分潮解的NaOH固体配制溶液 |
| B、将NaOH固体溶解后立即注入容量瓶配制溶液 |
| C、容量瓶中原来就有少量蒸馏水 |
| D、定容观察时俯视液面 |
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(甲苯) | 酸性KMnO4溶液 | 分液 |
| B | 甲烷(乙烯) | 饱和溴水 | 洗气 |
| C | 乙醇(乙酸) | CaO | 蒸馏 |
| D | 溴苯(溴) | 苯、铁粉 | 过滤 |
| A、A | B、B | C、C | D、D |
下列有关苯酚的实验事实中,能说明侧链对苯环性质有影响的是( )
| A、苯酚能与氢气加成生成环己醇 |
| B、苯酚能和NaOH溶液反应 |
| C、苯酚燃烧产生带浓烟的火焰 |
| D、苯酚与浓溴水反应生成三溴苯酚 |
相同质量的氯酸钾分别发生如下反应:①2KClO3
2KCl+3O2↑ ②4KClO3
KCl+3KClO4下列关于的说法不正确的是( )
| ||
| ||
| A、都氧化还原反应 |
| B、发生还原反应的元素相同 |
| C、发生氧化反应的元素相同 |
| D、发生电子转移的数目不同 |
 元素周期表中,金属和非金属分界线附近的元素性质特殊.其单质和化合物应用广
元素周期表中,金属和非金属分界线附近的元素性质特殊.其单质和化合物应用广