题目内容
下列表述中正确的是( )
| A、金属易锈蚀能用金属的电子气理论加以解释 |
| B、化学式Si02能真实表示物质分子组成 |
| C、共价键、离子键和范德华力都是微粒之间的不同作用力,Na2O2、石墨、白磷均含有上述两种作用力 |
| D、CCl4与KCl晶体中,化学键种类相同,晶体类型也相同 |
考点:金属晶体,不同晶体的结构微粒及微粒间作用力的区别,硅和二氧化硅
专题:化学键与晶体结构,元素及其化合物
分析:A.金属的化学性质比较活泼,容易被空气中的氧气所氧化,金属易锈蚀与金属晶体结构无关、与化学性质有关;
B.Si02为原子晶体;
C.活泼金属和活泼的非金属之间形成的键大多是离子键,离子晶体中含有离子键,可能含有共价键;大多非金属元素之间形成的键是共价键,以共价键结合的物质可能为原子晶体,也可能为分子晶体,在分子晶体中还存在分子间作用力;分子晶体含有范德华力,石墨为混合型晶体;
D.活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,根据晶体的构成微粒确定晶体类型.
B.Si02为原子晶体;
C.活泼金属和活泼的非金属之间形成的键大多是离子键,离子晶体中含有离子键,可能含有共价键;大多非金属元素之间形成的键是共价键,以共价键结合的物质可能为原子晶体,也可能为分子晶体,在分子晶体中还存在分子间作用力;分子晶体含有范德华力,石墨为混合型晶体;
D.活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,根据晶体的构成微粒确定晶体类型.
解答:
解:A.金属易锈蚀与金属晶体结构无关、与化学性质有关,金属的化学性质比较活泼,容易被空气中的氧气所氧化,故金属易腐蚀不能用金属晶体结构加以解释,故A错误;
B.Si02为原子晶体,是由硅原子和氧原子以共价键构成的空间网状结构,没有Si02分子,故B错误;
C.石墨是层状结构,层内碳原子之间形成共价键,层与层之间通过分子间作用力结合;Na+和O22-之间形成离子键、O22-中氧原子之间形成共价键;白磷分子内磷原子之间形成共价键,而分子与分子间为范德华力,故C正确;
D.CCl4中存在共价键,由分子构成的,为分子晶体,KCl中只存在离子键,为离子晶体,故D错误.
故选C.
B.Si02为原子晶体,是由硅原子和氧原子以共价键构成的空间网状结构,没有Si02分子,故B错误;
C.石墨是层状结构,层内碳原子之间形成共价键,层与层之间通过分子间作用力结合;Na+和O22-之间形成离子键、O22-中氧原子之间形成共价键;白磷分子内磷原子之间形成共价键,而分子与分子间为范德华力,故C正确;
D.CCl4中存在共价键,由分子构成的,为分子晶体,KCl中只存在离子键,为离子晶体,故D错误.
故选C.
点评:本题考查化学键和晶体类型,难度不大,注意化学键的形成规律及分子晶体中存在分子间作用力,石墨结构是学生的易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在密闭恒容容器中,可逆反应A(g)+B(g)?3C(g)△H<0达平衡时,下列说法不正确的是( )
| A、通入稀有气体使压强增大,平衡将逆向移动 |
| B、C的正反应速率是A的逆反应速率的3倍 |
| C、降低温度,混合气体的平均相对分子质量减小 |
| D、移走部分C,C的体积分数减小 |
 如图表示反应X(g)+Y(g)?Z(g);△H<0,从时间0~t3s的变化,则t2~t3时间段的变化是由下列哪项条件的改变引起的( )
如图表示反应X(g)+Y(g)?Z(g);△H<0,从时间0~t3s的变化,则t2~t3时间段的变化是由下列哪项条件的改变引起的( )| A、升高温度 |
| B、迅速缩小容器体积 |
| C、增大X的浓度 |
| D、增大Y的浓度 |
23g金属钠(发生反应2Na+2H2O=2NaOH+H2↑)溶于多少克水中,可使所得溶液中Na+与水分子个数之比为1:10( )
| A、18g | B、180g |
| C、198g | D、162g |
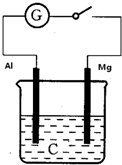 如图所示,把电极Al、Mg插入C的溶液中设计原电池.
如图所示,把电极Al、Mg插入C的溶液中设计原电池. 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题: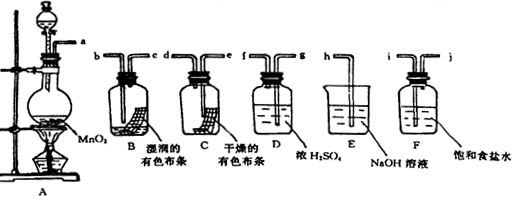
 是烯烃与H2加成的产物,则该烯烃可能有
是烯烃与H2加成的产物,则该烯烃可能有