题目内容
(6分)(1)甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.0 kJ·mol-1
CO(g)+3H2(g) ΔH=+206.0 kJ·mol-1
Ⅱ:CO(g)+2H2(g) CH3OH(g) ΔH=-129.0 kJ·mol-1
CH3OH(g) ΔH=-129.0 kJ·mol-1
CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为 _____________。
(2)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+ 氧化成Co3+,然后以Co3+ 作氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置模拟上述过程:

①写出阳极电极反应式 _______ 。
②写出Co3+除去甲醇的离子方程式 。
(6分) (1) CH4(g)+H2O(g) CH3OH(g)+H2(g) ΔH=+77.0 kJ·mol-1
CH3OH(g)+H2(g) ΔH=+77.0 kJ·mol-1
(2)①Co2+ — e-  Co3+ ②6Co3++CH3OH+H2O
Co3+ ②6Co3++CH3OH+H2O CO2↑+6Co2++6H+
CO2↑+6Co2++6H+
【解析】
试题分析:(1)根据盖斯定律,I+II可得所求的热化学方程式,所以CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为CH4(g)+H2O(g) CH3OH(g)+H2(g) ΔH=+77.0 kJ·mol-1;
CH3OH(g)+H2(g) ΔH=+77.0 kJ·mol-1;
(2)①阳极发生氧化反应,则Co2+ 被氧化成Co3+,电极反应式为Co2+ — e-  Co3+;
Co3+;
②Co3+ 作氧化剂把水中的甲醇氧化成CO2而净化,本身又被还原为Co2+,所以Co3+除去甲醇的离子方程式是6Co3++CH3OH+H2O CO2↑+6Co2++6H+。
CO2↑+6Co2++6H+。
考点:考查离子方程式的书写,盖斯定律的应用


 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 。
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 。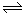 2SO3(g) △H=-197kJ/mol。在相同温度下,向密闭容器通入2mol SO2和1mol O2达平衡时,放热Q1;向另一相同体积的密闭容器中通入1mol SO2和0.5mol O2达平衡时,放出热量Q2,则下列关系式正确的是
2SO3(g) △H=-197kJ/mol。在相同温度下,向密闭容器通入2mol SO2和1mol O2达平衡时,放热Q1;向另一相同体积的密闭容器中通入1mol SO2和0.5mol O2达平衡时,放出热量Q2,则下列关系式正确的是 2R(g)+Q(g)反应达到平衡时,测得X和Y的转化率分别为30%和60%,则化学方程式中的n值为
2R(g)+Q(g)反应达到平衡时,测得X和Y的转化率分别为30%和60%,则化学方程式中的n值为