题目内容
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法不正确的是( )
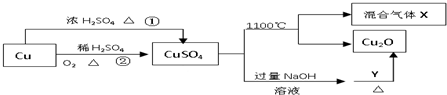

| A、相对于途径①,途径②更好地体现了绿色化学思想 |
| B、Y可以是葡萄糖溶液 |
| C、CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 |
| D、将CuSO4溶液蒸发浓缩,冷却结晶可制得胆矾晶体 |
考点:铜金属及其重要化合物的主要性质
专题:几种重要的金属及其化合物
分析:A.根据反应物和生成物的化学式判断,途径①产生二氧化硫气体污染性气体;
B、硫酸铜与氢氧化钠生成氢氧化铜沉淀,与Y生成氧化亚铜,知Y可为葡萄糖,因葡萄糖中有醛基;
C.硫酸铜分解生成Cu2O与氧气、SO2、SO3,依据电子守恒分析;
D.将CuSO4溶液蒸发浓缩、冷却结晶,过滤洗涤可制得胆矾晶体.
B、硫酸铜与氢氧化钠生成氢氧化铜沉淀,与Y生成氧化亚铜,知Y可为葡萄糖,因葡萄糖中有醛基;
C.硫酸铜分解生成Cu2O与氧气、SO2、SO3,依据电子守恒分析;
D.将CuSO4溶液蒸发浓缩、冷却结晶,过滤洗涤可制得胆矾晶体.
解答:
解:A.相对于途径①、③,铜和浓硫酸反应会生成二氧化硫气体污染空气,途径②的优点:制取等质量胆矾需要的硫酸少、途径②无污染性气体产生,更好地体现了绿色化学思想,故A正确;
B.葡萄糖与氢氧化铜反应的方程式为:C6H12O6+2Cu(OH)2=C6H12O7+Cu2O+2H2O,所以Y可为葡萄糖,故B正确;
C. 硫酸铜分解生成Cu2O与氧气、SO3、SO2,根据2CuSO4═Cu2O+SO2↑+SO3↑+O2↑知,X可能是O2、SO2和SO3的混合气体,若只是二氧化硫和三氧化硫,铜元素、氧元素化合价只有降低,无元素化合价升高,故C错误;
D.将CuSO4溶液蒸发浓缩、冷却结晶,过滤洗涤可制得胆矾晶体,故D正确;
故选C.
B.葡萄糖与氢氧化铜反应的方程式为:C6H12O6+2Cu(OH)2=C6H12O7+Cu2O+2H2O,所以Y可为葡萄糖,故B正确;
C. 硫酸铜分解生成Cu2O与氧气、SO3、SO2,根据2CuSO4═Cu2O+SO2↑+SO3↑+O2↑知,X可能是O2、SO2和SO3的混合气体,若只是二氧化硫和三氧化硫,铜元素、氧元素化合价只有降低,无元素化合价升高,故C错误;
D.将CuSO4溶液蒸发浓缩、冷却结晶,过滤洗涤可制得胆矾晶体,故D正确;
故选C.
点评:本题考查了物质的制备,解题的关键是掌握物质的性质,解答时要依据题干提供信息,结合相关知识细心分析解答,题目难度中等.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案
相关题目
以下元素基态原子电子排布图正确的是( )
A、 |
B、 |
C、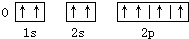 |
D、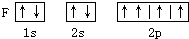 |
对于下列装置所示的实验,有关说法正确的是( )
A、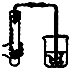 双手移去后,导管中水面与烧杯水面相平,则说明装置不漏气 |
B、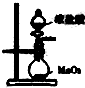 用于实验室制取Cl2 |
C、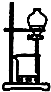 从海带中提取碘的实验过程中,用如图装置向烧杯中放出碘的苯溶液 |
D、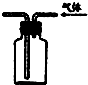 可用于实验室收集甲烷气体 |
下列有关溶液组成的描述合理的是( )
| A、无色溶液中可能大量存在Al3+、NH4+、Cl-、S2- |
| B、酸性溶液中可能大量存在Na+、ClO-、SO42-、I- |
| C、弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- |
| D、中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- |