题目内容
MgCO3中滴加盐酸的化学方程式为: .
考点:镁、铝的重要化合物
专题:几种重要的金属及其化合物
分析:碳酸镁与盐酸的反应类似于碳酸钙与盐酸的反应,反应生成氯化镁、水、及二氧化碳.
解答:
解:碳酸镁与盐酸的反应符合碳酸盐与酸的反应规律,产物为氯化镁、水、及二氧化碳,化学反应为MgCO3+2HCl═MgCl2+CO2↑+H2O,
故答案为:MgCO3+2HCl═MgCl2+CO2↑+H2O.
故答案为:MgCO3+2HCl═MgCl2+CO2↑+H2O.
点评:本题考查化学方程式的书写,明确反应规律是解题的关键.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法不正确的是( )
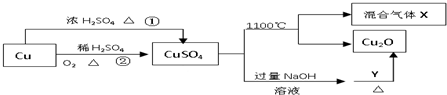

| A、相对于途径①,途径②更好地体现了绿色化学思想 |
| B、Y可以是葡萄糖溶液 |
| C、CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 |
| D、将CuSO4溶液蒸发浓缩,冷却结晶可制得胆矾晶体 |
能实现Al3++3AlO2-+6H2O=4Al(OH)3↓过程的是( )
| A、向铝盐溶液中不断滴加氢氧化钠溶液 |
| B、向偏铝酸盐溶液中不断加入盐酸 |
| C、向偏铝酸钠溶液中不断通入二氧化碳气体 |
| D、向氢氧化钠溶液中不断滴加铝盐溶液 |
室温时,0.1mol?L-1的HA溶液的pH=3,向该溶液中逐滴加入0.1mol?L-1 NaOH溶液,在滴加过程中,有关叙述正确的是( )
| A、未加入NaOH溶液时,原HA溶液中c(H+)=c(OH-)+c(A-) |
| B、向原溶液中滴入少量NaOH溶液,离子浓度可能为:c(A-)>c(Na+)>c(H+)>c(OH-) |
| C、当滴入的NaOH与HA恰好完全中和时,溶液中c(Na+)=c(A-) |
| D、当加入过量的NaOH溶液时,溶液可能呈中性,也可能呈碱性 |