题目内容
在一个恒温容积为2L的恒容容器中加入3mol的H2和2mol的CO,当反应2H2(g)+CO(g)═CH3OH(g)达到平衡时,测得容器内的压强是反应前压强的
,该温度下反应的平衡常数为 .
| 3 |
| 5 |
考点:化学平衡的计算
专题:化学平衡专题
分析:依据化学平衡三段式列式计算,达到平衡状态,测得容器内的压强是反应前压强的
,据此列方程求解.
2H2(g)+CO(g)?CH3OH(g)
起始量(mol) 3 2 0
变化量(mol) 2X X X
平衡量(mol) 3-2X 2-X X
平衡常数概念是生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积.
| 3 |
| 5 |
2H2(g)+CO(g)?CH3OH(g)
起始量(mol) 3 2 0
变化量(mol) 2X X X
平衡量(mol) 3-2X 2-X X
平衡常数概念是生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积.
解答:
解:达到平衡状态,测得容器内的压强是反应前压强的
,据此列方程求解:
2H2(g)+CO(g)?CH3OH(g)
起始量(mol) 3 2 0
变化量(mol) 2X X X
平衡量(mol) 3-2X 2-X X
根据测得容器内的压强是反应前压强的
得,
=
,X=1,
反应的平衡常数K=
=
=4(L/mol)2,该反应的平衡常数为4(L/mol)2,
故答案为:4(L/mol)2.
| 3 |
| 5 |
2H2(g)+CO(g)?CH3OH(g)
起始量(mol) 3 2 0
变化量(mol) 2X X X
平衡量(mol) 3-2X 2-X X
根据测得容器内的压强是反应前压强的
| 3 |
| 5 |
| 3-2X+2-X+X |
| 3+2 |
| 3 |
| 5 |
反应的平衡常数K=
| C(CH 3OH) |
| C(H 2) 2C(CO) |
| 1mol/2L |
| (1mol/2L)×(1mol/2L)2 |
故答案为:4(L/mol)2.
点评:本题考查了化学平衡的三段式计算应用,平衡常数概念的计算分析是解题关键,题目难度中等.

练习册系列答案
相关题目
可以用来鉴别Cl-、Br-、I-离子的是( )
| A、AgNO3溶液和稀硝酸 |
| B、观察它们的颜色 |
| C、用焰色反应进行实验 |
| D、分别向里滴加氯水 |
“厨房化学”是指利用家庭生活用品来进行化学实验,从而对化学进行学习和探究的活动.下列实验在厨房中不能完成的是( )
| A、检验鸡蛋壳中含有碳酸盐 |
| B、检验蛋白质在加热条件下能发生变性 |
| C、检验加碘食盐中不含碘单质 |
| D、检验自来水中含有Cl-离子 |
200℃时,11.6g CO2和水蒸气的混合气与过量的Na2O2充分反应后,固体质量增加了3.6g,再将反应后剩余固体冷却后加入含有Na+、HCO3-、SO32-、CO32-等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是( )
| A、原混合气体的平均摩尔质量为23.2g/mol |
| B、混合气体与Na2O2反应过程中电子转移的物质的量为0.25mol |
| C、溶液中SO32-的物质的量浓度基本保持不变 |
| D、溶液中HCO3-的物质的量浓度减小,CO32-的物质的量浓度增大,但是加入“剩余固体”充分反应后溶液中HCO3-和CO32-的物质的量浓度之和与加入“剩余固体”前基本保持不变 |
“碧水千河扬长帆,蓝天白云飘纸鸢.草长莺飞千山绿,人与江山共画卷.”我们淮安市人民正在积极建设“碧水蓝天”的生态城市,下列措施中不合理的是( )
| A、限制化学工业发展,关停所有化工企业,消除污染源头 |
| B、积极推广太阳能、风能等新能源的使用,减少化石燃料的使用 |
| C、加强城市生活污水脱氮除磷处理,遏制水体富营养化 |
| D、禁止农村燃烧秸杆,积极推广沼气、秸秆发电、秸秆制乙醇等实用技术的使用 |
下列有关实验原理、装置、操作或结论的描述中,正确的是( )
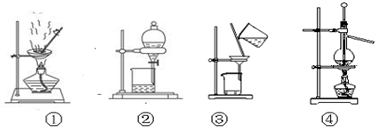

| A、用图①装置蒸发稀盐酸制浓盐酸 |
| B、用图②装置分液时,下层液体从分液漏斗下口放出,关闭活塞再将上层液体从上口倒出 |
| C、用图③洗涤沉淀时,漏斗中加入适量蒸馏水,搅拌并滤干 |
| D、用图④装置,分离四氯化碳与苯的混合溶液 |
