题目内容
16.800℃时,a、b、c三种气态物的浓度随时间变化的情况如图,由图分析不能得出的结论是( )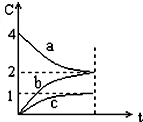
| A. | a是反应物 | B. | 正反应是一个体积扩大的反应 | ||
| C. | 正反应是放热反应 | D. | 若增大压强,平衡逆向移动 |
分析 根据图象可知,达到平衡时a的浓度减小2个单位,b的浓度增大2个单位,c的浓度增大1个单位,据此可知该反应的方程式为:2a(g)?2b(g)+c(g),据此结合化学平衡的影响因素进行解答.
解答 解:根据图象可知,达到平衡时a的浓度减小2个单位,b的浓度增大2个单位,c的浓度增大1个单位,据此可知该反应的方程式为:2a(g)?2b(g)+c(g),
A.根据分析可知,a为反应物,故A正确;
B.该反应中,反应物总体积为2,生成物总体积为3,则正反应是体积增大的反应,故B正确;
C.根据图象无法判断该反应是吸热反应还是放热反应,故C错误;
D.该反应为气体体积增大的反应,增大压强后平衡向着逆向移动,故D正确;
故选C.
点评 本题考查了化学平衡及其影响,题目难度不大,根据图象数据确定该反应方程式为解答关键,注意熟练掌握影响化学平衡的因素,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
7.下列化学用语正确的是( )
| A. | H2S的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{S}}{••}$${\;}_{•}^{•}$]2-H+ | |
| B. | Mg2+的结构示意图: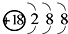 | |
| C. | Na2O的电子式:Na${\;}_{2}^{+}$[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2- | |
| D. | N2的电子式: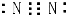 |
4.下列溶液中的Cl-浓度与1mol/LMgCl2溶液中的Cl-浓度相等的是( )
| A. | 1mol/L NaCl溶液 | B. | 1 mol/LCaCl2溶液 | ||
| C. | 1 mol/L KCl溶液 | D. | 1 mol/LAlCl3溶液 |
11.从平时学生实验中我们发现,同学们在进行实验时出现许多不正确的操作方式,希望同学们在今后的实验中,应该克服不规范的操作.请找出下列图示中正确的实验操作( )
| A. | 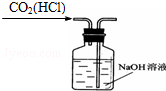 除去CO2中的HCl | B. | 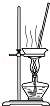 蒸发氯化钠溶液 | ||
| C. | 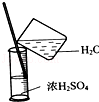 稀释浓硫酸 | D. | 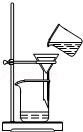 过滤 |
8.关于碱金属的叙述不正确的是( )
| A. | 熔点:Li>Na>K>Rb>Cs | |
| B. | 碱性:LiOH<NaOH<KOH<RbOH<CsOH | |
| C. | 与水反应的剧烈程度:Li<Na<K<Rb<Cs | |
| D. | 都能在空气中燃烧生成R2O(R表示碱金属) |
5.a、b、c、d是四种短周期元素.a、b、d同周期,c、d同主族.a的原子结构示意图为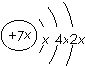 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为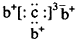 .下列比较中正确的是( )
.下列比较中正确的是( )
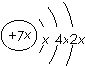 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为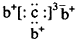 .下列比较中正确的是( )
.下列比较中正确的是( )| A. | 原子半径:a>c>d>b | B. | 非金属性 b>d>c | ||
| C. | 原子序数:d>a>c>b | D. | 最高价含氧酸的酸性c>d>a |
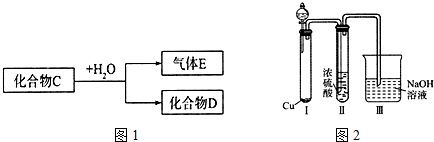
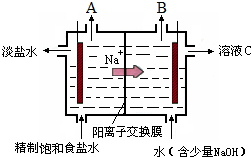 氯碱工业中电解饱和食盐水的原理示意图如图所示:
氯碱工业中电解饱和食盐水的原理示意图如图所示: