题目内容
12.下列说法正确的是( )| A. | N2、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| B. | 向AlCl3溶液中滴加过量的氨水能看到先产生白色沉淀,后沉淀溶解 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉就会溶解 | |
| D. | 可用浓硫酸或者浓硝酸除去镀在铝表面的铜镀层 |
分析 A.氮气不是大气污染物,且NO在空气中不能稳定存在;
B.氯化铝与氨水反应生成氢氧化铝沉淀,但是氢氧化铝不溶于氨水;
C.硝酸根离子在酸性条件下具有强氧化性,能够氧化铜;
D.浓硫酸不与铜反应,不能用浓硫酸除去铜.
解答 解:A.NO、NO2为大气污染物,而N2不是大气污染物,NO在空气中不能稳定存在,故A错误;
B.向AlCl3溶液中滴加过量的氨水能看到先产生白色沉淀,但是氨水为弱碱,氨水过量后沉淀不会溶解,故B错误;
C.在稀硫酸中加入铜粉,稀硫酸不与铜反应,则铜粉不溶解;再加入Cu(NO3)2固体,硝酸根离子在酸性条件下能够氧化铜,则铜粉就会溶解,故C正确;
D.可用浓硝酸除去镀在铝表面的铜镀层,常温下铜不与浓硫酸反应,则不能用浓硫酸除去铜,故D错误;
故选C.
点评 本题考查了铜及其化合物性质,题目难度中等,明确常见元素及其化合物性质为解答关键,注意硝酸根离子在酸性条件下具有强氧化性,为易错点,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
20.向含有c(FeCl3)=0.2mol•L-1、c(FeCl2)=0.1mol•L-1的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其中分散质粒子是直径约为9.3nm的金属氧化物,下列有关说法中正确的是( )
| A. | 该分散系的分散质为Fe2O3 | |
| B. | 在电场作用下,阴极附近分散系黑色变深,则说明该分散系带正电荷 | |
| C. | 加入NaOH时发生的反应可能为:Fe2++2Fe3++8OH-═Fe3O4+4H2O | |
| D. | 可用过滤的方法将黑色金属氧化物与Na+分离开 |
4.在恒温恒容条件下,发生化学反应H2 (g)+I2(g)?2HI (g),下列选项中不能作为达到平衡状态标志的是( )
| A. | 混合气体颜色不再变化 | |
| B. | 单位时间内生成nmol氢气的同时生成nmol碘蒸气 | |
| C. | 若该反应在隔热密闭体积恒定的容器中进行反应,体系的温度不再变化 | |
| D. | 2v正(H2)=v逆(HI) |
11.下列叙述中,错误的是( )
| A. | 苯与浓硫酸共热并保持70-80℃反应生成苯磺酸 | |
| B. | 苯乙烯在合适条件下催化加氢可生成乙基环己烷 | |
| C. | 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 | |
| D. | 甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 |


 C:CH2OHCH2OH
C:CH2OHCH2OH E:
E:
 .
. .
.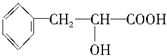
 (只要求写出一个化学方程式,有机物写结构简式).
(只要求写出一个化学方程式,有机物写结构简式).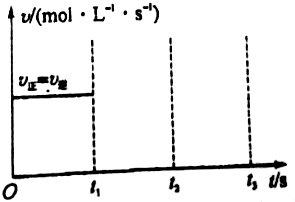 工业上制硫酸的第二步反应:2SO2(g)+O2(g)?2SO3(g)△H<0,在一定条件下通入2mol SO2(g)和1mol O2(g)达到平衡时,其反应速率关系如图所示.维持温度、压强不变,在t1时刻充入2mol SO3(g),t2时反应达到新的平衡.请画出t1~t3正、逆反应速率v正、v逆的变化示意图.
工业上制硫酸的第二步反应:2SO2(g)+O2(g)?2SO3(g)△H<0,在一定条件下通入2mol SO2(g)和1mol O2(g)达到平衡时,其反应速率关系如图所示.维持温度、压强不变,在t1时刻充入2mol SO3(g),t2时反应达到新的平衡.请画出t1~t3正、逆反应速率v正、v逆的变化示意图.