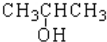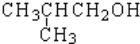题目内容
1.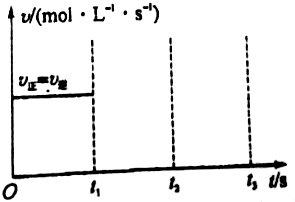 工业上制硫酸的第二步反应:2SO2(g)+O2(g)?2SO3(g)△H<0,在一定条件下通入2mol SO2(g)和1mol O2(g)达到平衡时,其反应速率关系如图所示.维持温度、压强不变,在t1时刻充入2mol SO3(g),t2时反应达到新的平衡.请画出t1~t3正、逆反应速率v正、v逆的变化示意图.
工业上制硫酸的第二步反应:2SO2(g)+O2(g)?2SO3(g)△H<0,在一定条件下通入2mol SO2(g)和1mol O2(g)达到平衡时,其反应速率关系如图所示.维持温度、压强不变,在t1时刻充入2mol SO3(g),t2时反应达到新的平衡.请画出t1~t3正、逆反应速率v正、v逆的变化示意图.
分析 维持温度、压强不变,在t1时刻充入2mol SO3(g),体积膨胀,从起始到t1时刻反应物的浓度减小,生成物的浓度增加,正反应速率瞬间减小,然后逐渐增大,逆反应速率逐渐增大,然后逐渐减小,于t2时刻达到新的平衡,依此作图为: ,由此作答.
,由此作答.
解答 解:维持温度、压强不变,在t1时刻充入2mol SO3(g),体积膨胀,从起始到t1时刻反应物的浓度减小,生成物的浓度增加,正反应速率瞬间减小,然后逐渐增大,逆反应速率逐渐增大,然后逐渐减小,于t2时刻达到新的平衡,且最终与原平衡是等效平衡,依此作图为 ,故答案为:
,故答案为: .
.
点评 本题考查了反应速率图象,学生要清楚在维持温度、压强不变,相当于体积可变,最终与原平衡是等效平衡,侧重于考查学生的综合能力,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.下列说法正确的是( )
| A. | N2、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| B. | 向AlCl3溶液中滴加过量的氨水能看到先产生白色沉淀,后沉淀溶解 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉就会溶解 | |
| D. | 可用浓硫酸或者浓硝酸除去镀在铝表面的铜镀层 |
16.25℃时,在某澄清透明酸性溶液中,则在此溶液中还能大量共存的离子组有( )
| A. | Na+、Fe2+、NO3- | B. | K+、ClO-、SO42- | ||
| C. | NH4+、HCO3-、AlO2- | D. | Cu2+、Mg2+、Cl- |
6.盐酸在不同的反应中,可以分别表现出酸性、氧化性和还原性.现在有如下三个反应,有关判断正确的是( )
①Zn+2HCl═ZnCl2+H2↑
②NaOH+HCl═NaCl+H2O
③2HCl$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑
①Zn+2HCl═ZnCl2+H2↑
②NaOH+HCl═NaCl+H2O
③2HCl$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑
| A. | 反应①是置换反应,HCl表现还原性 | |
| B. | 反应②是复分解反应,HCl表现氧化性 | |
| C. | 反应③中HCl既有氧化性也有还原性 | |
| D. | 反应①中氧化剂和氧化产物的物质的量之比是1:1 |
2.“绿色化学”要求从根本上减少乃至杜绝污染.下列对我们学习使用的纸张的处理方法,不符合“绿色化学”的是( )
| A. | 一纸多用,尽量提高纸张的使用效率 | |
| B. | 回收处理,不乱扔、乱丢废纸屑 | |
| C. | 在高浓度氧气中燃烧,不产生废弃物 | |
| D. | 积累、保存送造纸厂处理 |
19.下列不能水解的糖类是( )
| A. | 纤维素 | B. | 果糖 | C. | 麦芽糖 | D. | 淀粉 |
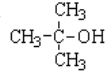
20.烷烃 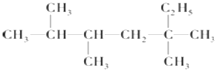 是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )
是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )
 是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )
是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )| A. | 4种 | B. | 7种 | C. | 6种 | D. | 5种 |
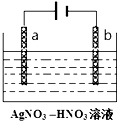 如图为含有少量Zn杂质的粗银电解精炼银的示意图
如图为含有少量Zn杂质的粗银电解精炼银的示意图