题目内容
18.将4.6g钠用铝箔包住投入到足量水中,充分反应后,产生的气体标准状况下的体积是( )| A. | 11.2L | B. | 2.24L | C. | 3.36L | D. | 8.96L |
分析 发生反应:2Na+2H2O═2NaOH+H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑,一般考虑铝箔过量,根据方程式计算生成生成氢气的物质的量,再根据V=nVm计算氢气体积.
解答 解:4.6gNa的物质的量为$\frac{4.6g}{23g/mol}$=0.2mol,
2Na+2H2O═2NaOH+H2↑
0.2mol 0.2mol 0.1mol
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
0.2mol 0.3mol
故生成氢气体积为(0.1mol+0.3mol)×22.4L/mol=8.96L,
故选D.
点评 本题考查化学方程式有关计算,明确发生的反应即可解答,有利于基础知识的巩固.

练习册系列答案
相关题目
13.已知氢气的燃烧热为285.8kJ/mol,CO的燃烧热为282.8kJ/mol;现有H2和CO组成的混合气体56.0L(标准状况),经充分燃烧后,放出总热量为710.0kJ,并生成液态水.下列说法正确的是( )
| A. | CO燃烧的热化学方程式为:2CO(g)+O2(g)=2CO2(g)△H=+285.8kJ/mol | |
| B. | H2燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(g)△H=-571.6kJ/mol | |
| C. | 燃烧前混合气体中H2的体积分数为40% | |
| D. | 燃烧后的产物全部与足量的过氧化钠作用可产生1.25mol氧气 |
6.第16届亚运会于2010年11月12日至27日在中国广州进行.其火炬“潮流”的外壳主要采用高品质的铝合金材料制造,在其燃烧系统内装有主要成分为丙烷的环保型燃料.下列有关丙烷的叙述中,不正确的是( )
| A. | 丙烷是直链烃,但分子中碳原子不在一条直线上 | |
| B. | 在光照条件下,丙烷能够与氯气发生取代反应 | |
| C. | 丙烷比其同分异构体丁烷易汽化,耗氧量少 | |
| D. | 丙烷燃烧时主要是将化学能转变为热能和光能 |
13.下列各组物质中,分子数一定相同的是( )
| A. | 2L CO和2L CO2 | B. | 1mol O2和标况下22.4L H2O | ||
| C. | 0.2mol H2O和4.48L HCl气体 | D. | 9g H2O和0.5mol CO2 |
3. 2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )
2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )
 2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )
2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )| A. | 合金的熔点通常比组分金属高,硬度比组分金属小 | |
| B. | 已知Ga处于ⅢA族,可推知氮化镓化学式为Ga3N2 | |
| C. | 用金属铝与V2O5冶炼钒,铝作还原剂 | |
| D. | 合金的化学性质一般与其各成分金属的化学性质不同 |
7.下列溶液中一定呈中性的是( )
| A. | pH=7的溶液 | B. | c(H+)=c(OH-)=10-6mol•L-1的溶液 | ||
| C. | 能够与Na反应生成H2的溶液 | D. | 电解食盐水最后所得溶液 |
8.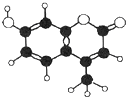 羟甲香豆素是一种激光染料,应用于可调谐染料激光器.羟甲香豆素分子模型如图所示,下列有关叙述错误的是( )
羟甲香豆素是一种激光染料,应用于可调谐染料激光器.羟甲香豆素分子模型如图所示,下列有关叙述错误的是( )
 羟甲香豆素是一种激光染料,应用于可调谐染料激光器.羟甲香豆素分子模型如图所示,下列有关叙述错误的是( )
羟甲香豆素是一种激光染料,应用于可调谐染料激光器.羟甲香豆素分子模型如图所示,下列有关叙述错误的是( )| A. | 能使高锰酸钾溶液褪色 | |
| B. | 能与溴水发生取代反应和加成反应 | |
| C. | 分子式为C10H9O3 | |
| D. | 1mol羟甲香豆素最多能与3molNaOH反应 |
 磷酸铁锂动力电池(LiFePO4电池)的内部结构如图所示.中间是聚合物的隔膜,它把正极与负极隔开,锂离子可以通过而电子不能通过.该电池的总反应式为:Li1-xFePO4+LixC6═C6+LiFePO4
磷酸铁锂动力电池(LiFePO4电池)的内部结构如图所示.中间是聚合物的隔膜,它把正极与负极隔开,锂离子可以通过而电子不能通过.该电池的总反应式为:Li1-xFePO4+LixC6═C6+LiFePO4
 A→F
A→F