题目内容
用13.5Al与足量HCl反应生成的氢气的分子数是 .
考点:化学方程式的有关计算
专题:
分析:铝和盐酸反应生成氯化铝和氢气,根据铝的质量计算氢气的物质的量,再根据N=n×NA计算分子数.
解答:
解:2Al+6HCl=AlCl3+3H2↑
54g 3mol
13.5g n
n=
=0.75mol,
N=0.75mol×NA/mol=0.75NA;
故答案为:0.75NA.
54g 3mol
13.5g n
n=
| 13.5g×3mol |
| 54g |
N=0.75mol×NA/mol=0.75NA;
故答案为:0.75NA.
点评:本题考查了化学方程式的计算,较简单,注意解题格式.

练习册系列答案
相关题目
某溶液中只可能含有下列离子中的几种(不考虑溶液中含的较少的H+和OH-):Na+、NH4+、SO42-、CO32-、NO3-.取200mL该溶液,分为等体积的两份分别做下列实验.实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL.实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g.下列说法正确的是( )
| A、该溶液中一定含有Na+,且c(Na+)≥0.1 mol?L-1 |
| B、该溶液中可能含有Na+ |
| C、该溶液中一定不含NO3- |
| D、该溶液中肯定含有NH4+、SO42-、CO32-、NO3- |
一支规格为AmL的酸式滴定管,其尖咀部分充满液体时,液面在mmL刻度处,当液面降低到nmL刻度处时,下列判断正确的是( )
| A、流出的流体的体积是(m-n)mL |
| B、流出的液体的体积是(n-m)mL |
| C、滴定管内剩余的液体的体积是(A-n)mL |
| D、滴定管内剩余的液体的体积大于(A-n)mL |
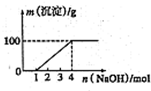 某澄清透明溶液中只可能含有①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥CO32-;⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示.则该溶液中一定含有的离子是( )
某澄清透明溶液中只可能含有①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥CO32-;⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示.则该溶液中一定含有的离子是( )| A、③⑤⑦ | B、②③⑤⑦ |
| C、①②③⑥⑦ | D、①②③④⑤⑦ |
下列变化不可能通过一步实验直接完成的是( )
| A、Al(OH)3→Al2O3 |
| B、Al2O3→Al(OH)3 |
| C、Al→AlO2- |
| D、AlCl3→Al(OH)3 |
以石墨为电极,电解KI溶液(含有少量的酚酞和淀粉),下列说法错误的是( )
| A、阴极附近溶液呈红色 |
| B、阴极反应式与硫酸钠溶液时相同 |
| C、阳极附近溶液呈蓝色 |
| D、溶液的pH变小 |
下列变化中,不可能通过一步反应实现的是( )
| A、SiO2→Na2SiO3 |
| B、SiO2→H2SiO3 |
| C、CuSO4→CuCl2 |
| D、Cu(OH)2→CuO |